1. 서 론
시험·검사기관에서 시험방법을 적용하기에 앞서 시험방법이 시험의 목적에 적합한지를 검증하는 과정은 중요한 과정이며, ISO/IEC 17025 [
1]에서는 시험방법의 유효성 확인 과정을 중요시 하고 있다. 특히 국내·외 시험기관간의 정보공유, 공동연구 등의 연구 패러다임의 변화를 필요로 하는 시대에서는 단일 시험·검사기관의 시험방법, 연구자가 단독으로 개발한 시험기준 또는 방법에 대한 검증은 분석결과의 신뢰도를 확보하는데 중요한 툴이라 할 수 있다. 특히, 환경분야 시험·검사업무와 같이 시험·분석과정에서 생산되는 데이터들이 국민들의 생활에 밀접하게 영향을 미치는 분야에서는 그 중요성이 더 크다고 할 수 있다. 본 연구에서는 국내·외 여러 시험검사기관에서 운영하고 있는 시험검사방법의 유효성 확인 지침 또는 가이드라인을 조사하여 각각의 지침에서 제시한 유효성 확인 인자와 절차 등을 조사하였다. 국내자료는 국가기술표준원[
2]의 KOLAS 지침, 식품의약품안전처[
3]의 지침을 조사하였고, 국외자료는 EPA [
4], NATA [
5], UKAS [
6], Eurachem [
7], IUPAC [8]의 가이드라인을 조사하였다. 국가기술표준원(KOLAS)에서는「화학적 시험방법의 유효성 확인을 위한 지침」을 제정하여 활용도록 하고 있으며, 식품의약품안전처에서는「의약품등 밸리데이션 실시에 관한 규정」을 제정하여 의약품의 제조공정까지를 포함하여 공정, 시험방법, 세척, 제조지원 설비, 컴퓨터시스템 밸리데이션으로 구분하여 활용하도록 하고 있다. EPA는 Validation and peer review of US environmental protection agency (chemical method analysis)에서 환경분야의 이화학적 시험에서 생산되는 데이터들의 신뢰도 확보를 위한 Verification과 Validation과정을 제시하고 있다. 호주의 NATA는 시험기관에서 운영하고 있는 시험·검사 방법의 유효성 확인 과정에서 운영하고 있는 이화학적 시험방법의 검증 가이드라인을 지침으로 운영하고 있다. 이 지침에서는 시험방법의 유효성 확인과 관련된 흐름도 를 제시하여 매 과정마다 검토해야 되는 중요한 확인사항을 제시하고 있다. Eurachem에서도 성상확인시험(Identification test), 불순물에 대한 정량시험(Quantitative test for impurity), 성분에 대한 정량시험(Quantification of component)로 구분하고 있다. 영국의 UKAS는 시험·검사방법의 유효성검증은 ISO/IEC 17025를 지침을 따르도록 하고 있으며, 이 지침에서는 비표준화 시험방법을 적용할 때, 시험실에서 자체 개발한 시험방법을 적용할 때, 표준화된 시험방법을 다른 용도로 사용할 때, 시험자가 기존의 표준시험방법을 확장됨 방법 또는 수정된 방법으로 사용한 경우 등을 포함하도록 하고 있다. IUPAC에서도 시험방법의 유효성검증과 관련된 적용인자들로서 다른 시험·검사기관에서 적용하고 있는 파라미터들 보다 더 많은 인자들을 제시하고 있다. 본 연구에서는 이러한 국내·외 시험·검사기관의 국내·외 지침 또는 가이드라인에서 제시하고 있는 유효성 검증 파라미터(인자)들을 조사하여 시험검사방법의 유효성 확인지침 작성 시 참고하도록 하였다.
2. 연구 방법
국내·외 시험·검사기관에서 시험·검사방법의 유효성 검증과 관련된 지침 또는 가이드라인을 조사하였으며, 조사한 자료를 토대로 유효성 검증에서 중요한 평가되는 요소들을 비교하였다. 아울러 각각의 시험검사기관에서 운영하는 시험방법의 유효성검증 절차에 대해서도 검토하였다.
2.1. 국내 문헌 검토
시험방법의 유효성 확인 지침에 필요한 인자들의 비교를 위한 자료조사는 국내 시험·검사기관에서 사용하고 있는 유효성 확인 인자들과 절차를 조사하였다. 국내자료는 국가기술표준원과 식품의약품안전처의 지침과 절차 등을 검토하였다.
2.2. 국외 문헌 검토
유효성 검증과 관련된 국외 시험검사기관은 EPA, NATA, UKAS, Eurachem, IUPAC의 가이드라인을 비교하였다. 각각의 시험·검사기관에서 제시하는 유효성 확인 인자들과 검증절차를 조사하였다.
3. 결과 및 고찰
3.1. 국내 시험·검사기관의 시험방법유효성 지침 조사
3.1.1. 국기술표준원[2]
국가기술표준원에서는 환경분야 시험·검사 업무를 포함한 다른 분야의 시험업무 및 검사업무를 수행하는 기관에서 활용할 수 있는「화학적 시험방법의 유효성 확인을 위한 지침」을 제정하여 운영하고 있다. 이 지침에서는 시험방법을 적용하기에 앞서, 시험방법이 시험목적에 적합한지의 여부를 먼저 검증하고 고객이 이 방법을 통해 얻은 결과를 확신을 가지고 활용할 수 있도록 해야 한다는 명제를 전제로 하고 있다. 시험방법의 유효성 확인(Method Validation)은 구체적인 용도에 따른 특정한 요구사항의 만족에 대한 객관적인 증거를 제공하도록 규정하고 있다. 또한, 시험방법 유효성 확인은 KS Q ISO/IEC 17025에 대한 시험기관 인정의 기본적인 요구사항을 반영하고 있으며, 이 규격에 따라 인정을 받은 시험기관은 자체 개발하거나 표준 시험방법에서 수정한 모든 방법을 유효화하고 표준 시험방법을 검증하여 그들이 사용하는 모든 방법의 유효성을 입증해야 하도록 규정하고 있다. 유효성 검증의 실시 여부는 ①새로 개발된 자체적인 방법(In-house Method) ②시험기관에서 이미 유효성이 확인된 시험 절차 ③시험기관은 그들 자신이 보유한 시험조건 하에서 표준시험방법에 규정된 성능 특성들을 충족할 수 있는지 여부에 대한 판단이 필요할 때 실시하도록 규정하고 있다. 이러한 과정에서 활용하는 인자로서는 선택성(Selectivity), 직선성(Linearity), 감도(Sensitivity), 정확도(Accuracy), 정밀도(Precision), 진도(Trueness), 검출한계(LOD, Limit of Detection). 정량한계(LOQ, Limit of Qualification), 범위(Range), 둔감도(Ruggedness), 측정불확도(Measurement Uncertainty) 등을 제시하고 있다.
Fig. 1.
Data validation components in KOLAS.
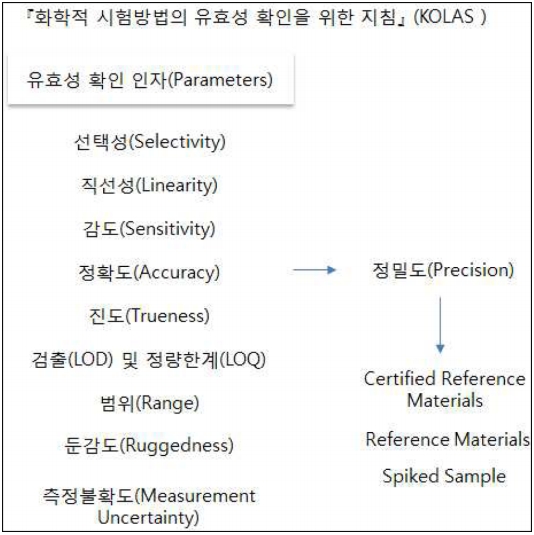
Table 1.
Summary of validation parameters of KOLAS [
2]
|
구분 |
주요내용 |
|
유효성 확인목적 |
측정 및 시험방법의 유효성확인의 첫 번째 단계는 무엇을 측정하고자 하는지를 정의하며, 측정할 대상에 대해 정성적인 기술 및 양(量)의 정의 및 고객의 요구사항에 대한 시험방법을 유효화할 때 수행함. |
|
주요인자 |
선택성(Selectivity), 직선성(Linearity), 매트릭스효과(Matrix effect), 감도(Sensitivity), 정확도(Accuracy), 정밀도(Precision), 진도(Trueness), 인증표준물질(CRM), 표준물질(RM), 첨가시료(Spiked samples), 범위(Range), 둔감도(Ruggedness), 측정불확도(Measurement uncertainty) |
Table 2.
Minimum or suggested number of experiments that should be performed by KOLAS [
2]
|
Parameter (주요인자) |
수행절차 |
분석 횟수 |
|
직선성 (Linearity) |
검량 표준의 분석 |
예상되는 시료의 농도 범위에 걸쳐 고르게 분포한 6 또는 그 이상의 표준에 대해 2회 반복 측정 |
|
감도 (Sensitivity) |
소량 첨가시료나 시료추출용액에 준비된 표준 시료의 분석 |
응답값 대 농도 좌표(Plot)에서 만족할 만한 기울기에 대한 초기 확인(초기확인 후에 QC 점검을 시행하는 것이 적합함). |
|
선택성 (Selectivity) |
잠재적인 간섭물질의 고려하여 가능한 양의 간섭물질을 첨가한 시료의 분석(시험방법 개발은 잠재적인 문제점을 극복할 수있다) |
필요하다면 1회의 시험으로 충분하다. |
|
진도(Trueness) 편의(Bias) |
- 다음을 분석 |
최소 7회 이상의 반복 분석 참조시료는 분석대상 시료와 매질 및 농도와 맞아야 한다. |
|
·CRM |
|
·기타 RM |
|
·첨가시료 |
|
- 표준 시험방법과의 비교 |
|
- 시험소간 공동연구 결과 |
|
정밀도 : 시험기관내에서의 재현성 |
시료의 반복 분석 ; 가능하다면 시험 결과의 사용자에게 가장 중요한 농도의 분석대상성분이 포함되도록 선택) |
각 매질 별로 최소 7회 이상의 반복 분석 |
|
LOD |
분석대상성분이 미량 함유된 시료의 분석 |
0에 근접한 농도가 포함된 3가지의 각 농도에서 최소 7회 이상의 반복 분석 (그래픽 방식), 또는 LOQ의 2배에 해당되는 농도에서 최소 7회 이상의 반복 분석(통계적 방식) |
|
LOQ |
※ 참고 : LOD 및 LOQ의 확인은 분석대상성분의 농도가 LOD나 LOQ와 비슷할 때 요구됨. |
각 매질 별로 다른 확인 절차가 필요할 수 있다. |
|
적용 범위 (Working Range) |
편의로부터의 자료 평가, 그리고 경우에 따라서 LOQ의 확인 |
|
|
둔감도 (Ruggedness) |
작은 변화가 발생할 경우 시험결과에 영향을 줄 수 있는 시험방법의 단계들을 고려 |
주의 깊게 관리하지 않는 경우 시험결과에 영향을 미칠 수 있는 변수에 대한 적절한 제한을 제공 하나의 변수에 작은 변경을 적용해서 시험 및 재시험 |
|
|
※ 필요 시, 다음을 조사 |
|
(i) 단일 변수 시험 |
|
(ii) 다중 변수 시험 |
|
측정 불확도 (Measurement Uncertainty) |
유효성 확인 데이터를 사용 가능한 기타 보충 자료 (예를들면 시험소간 공동연구, 숙련도시험, round robin 시험, 내부 QC 데이터)와 함께 활용한다. |
합리적이며 목적에 적합한 MU를 산정한다. 시험 결과의 사용자에게 가장 중요한 농도로 추정치를 조정 |
3.1.2 식품의약품안전처[3]
식품의약품안전처(이하, 식약처)에서는「약사법」, 「의약품 등의 안전에 관한 규칙」및「마약류에 관리에 관한 법률」에 따라서 의약품등 제조 및 품질관리에 적합성을 확인할 목적으로「의약품등 밸리데이션 실시에 관한 규정」을 제정하여 운영하고 있다. 이 지침에서는 의약품의 제조공정까지를 포함하여 ①공정 밸리데이션, ②시험방법 밸리데이션, ③세척 밸리데이션, ④제조지원 설비 밸리데이션, ⑤컴퓨터시스템 밸리데이션으로 구분하고 있다. 이 지침의 구성은 용어정의, 적격 성평가의 실시, 종류에 따른 밸리데이션 방법, 책임자 역할, 필요한 문서목록의 순서로 구성되어 있다. 이 규정에서는 다음과 같은 인자들을 유효성 확인 과정에서 활용하도록 정의하고 있다; 확인시험(Identification Test), 순도시험(Purity Test), 함량 또는 역가시험(Assay: Content or Potency), 특이성(Specificity), 정확도(Accuracy), 정밀도(Precision), 검출한계(Detection Limit), 정량한계(Quantitation Limit), 직선성(Linearity), 범위(Range), 완건성(Robustness). 정밀도(Precision)와 관련해서는 반복성(Repeatability), 실험실내 정밀도(Intermediate Precision), 실험실간 정밀도(Reproducibility)를 제시하고 있다. 유효성 확인의 적용범위와 인자들은
Table 3과
Table 4에 나타내었다.
Fig. 2.
Method validation parameters in Ministry of Food and Drug Safety.

3.2. 국외 시험·검사기관의 시험방법유효성 지침 조사
3.2.1 EPA [4]
미국 EPA는 Validation and peer review of US environmental protection agency(chemical method analysis)에서 환경시료의 이화학적 시험과정에서 생산되는 데이터들의 신뢰도 확보를 위한 Verification과 Validation과정을 정하고 있다. 특히 EPA지침에서는 Verification과 Validation과정을 분리하지 않고 연동시켜 검증하도록 제안하고 있다. Verification은 크게 5단계로 분류하여 계획수립(Project Planning)→현장업무(Fields Activities)→LIMS(시험실정보화시스템)→현장기록물의 검토(Fields Documentation Review)→데이터 검증(Data Verification Records and Verified data) 순으로 진행하도록 하고 있다. 이과정과 연계된 Validation과정은 현장과 시험실의 데이터 검증(Data validation of Field and analytical laboratory data)→데이터 유효성 확인 리포트 작성(Data validation report and validated data)→데이터 품질 검증(Data Quality Assessment)으로 진행하도록 하고 있다. 이와 더불어 특정한 데이터들 또는 외부에서 요구하는 데이터들의 품질관리를 위해서 집중데이터검증(Focused data validation)과정을 거치도록 하고 있다. 이 과정에서 사용하고 있는 파라미터들은 목적(purpose), 범위와 응용(Scope and Applicability), 선택성(Selectivity), 장비의 검정(Instrument calibration), 진도(Trueness), 정밀도(Precision), 정량한계 및 범위(Quantitation limits and ranges), 검출한계(Detection Limit), 둔감도(Ruggedness), 시험실상호간 평가(Inter Laboratory Study)로 구성되어 있다.
Fig. 3.
Data verification and data validation components in the project life cycle(EPA).
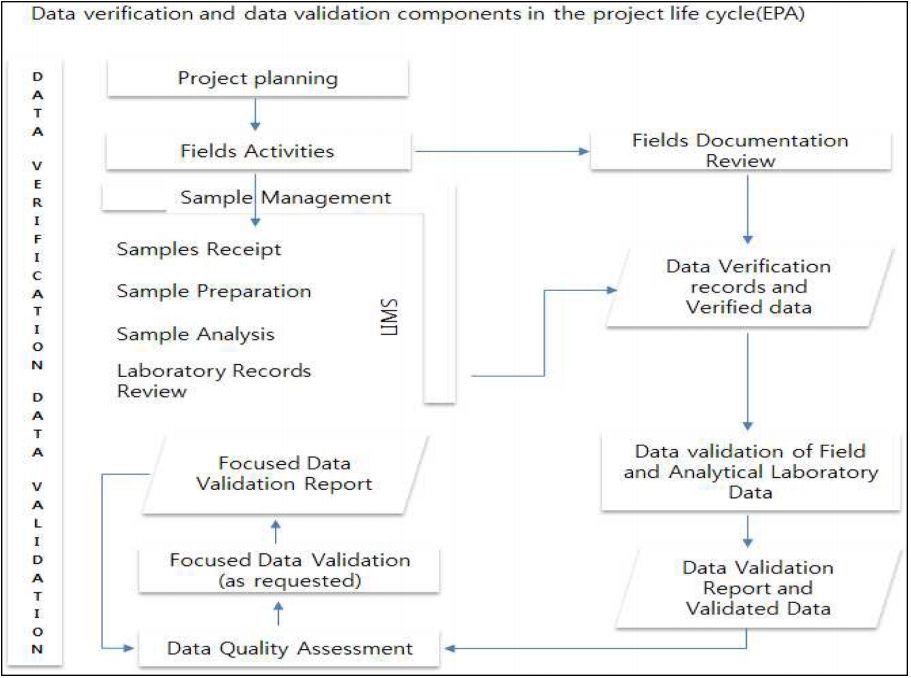
Table 5.
Definitions of method validation parameters and extent of validation works by the EPA
|
Parameter (주요인자) |
용어정의 또는 설명 |
|
Purpose (목적) |
방법은 시험검사의 목표 및 의도된 데이터의 용도를 명확하고 간결해야 하며 구체적인 설명을 포함하여야 함. |
|
Scope and Applicability (적용범위) |
범위 및 적용가능성은 방법의 적용가능 범위를 정의하는 역할을 함. 적용범위는 (a) 검증된 측정 프로세스 구성 요소, (b)분석대상 및 매트릭스의 특성, (c)해당시험법이 적합하다고 인정되는 분석대상 물질의 농도수준, (d) 적용될 시험방법에 근거한 기지 농도에 대한 기술 (e)분석과정의 변수가 품질목표를 충족시키는 지에 여부에 대한 설명 |
|
Selectivity (선택성) |
선택성은 시험방법에서 의도하는 분석물질, 농도수준 및 매트릭스로 부터 유용한 시험결과를 생산을 해야 함. 선택성은 관심대상 되는 분석물질을 복잡한 매트릭스 존재하에서 입증이 가능하여야 함. 선택성은 예상되는 매트릭스 성분 존재하에 분석물질의 검출가능성을 입증하여야 함. |
|
Instrument Calibration (장비검정) |
장비검정은 “Instrument linearity”에 포함시키기도 함. 넓은 의미에서는 분석장비 교정 및 검정모델의 특성을 나타내기도 하며, 시험방법의 유효성확인과정에서는 적용한 시험방법을 포함한 충분한 데이터를 검토하여야 함. |
|
Bias (편향)/Trueness (진도) |
Trueness(진도)는 분석과정의 오류원인을 나타내는 특성으로 볼 수 있으며, 바이어스(Bias)는 진도를 평가하는 척도의 하나임. 측정과정의 편차는 일반적으로 분석물질, 분석물질의 농도수준, 매트릭스에 따라 다르게 나타날 수 있으며, 접근방법으로는 참조자료(RM)의 사용, 대체방법의 선택 등이 있음. |
|
Precision (Repeatability and reproducibility) (정밀도) |
정밀도는 측정과정에서 임의 목표값으로 결집하는 능력을 반영하는 특성 중의 하나임. 몇 가지 유형의 정밀조사(예 : 반복성 및 재현성 시험)가 있으며, 요구사항의 준수 여부를 입증하기 위해 방법은 반복성(내부 실험실)과 재현성(실험실 간)에 대한 평가를 수행하여야 함. |
|
Quantitation range and Limits (정량범위) |
정량범위는 시험방법의 유효성 확인과정 중 측정의 정확도(진도 및 정밀도)를 특징으로 분석물질의 농도(또는 기타 양)를 정확하게 특징짓는 농도범위에 해당됨. |
|
Detection limits (검출한계) |
일반적으로 이 용어는 명확하게 식별(분석)할 수 있는 분석 물질의 최저수준을 나타냄. 검출한계는 특정 검출한계(주어진 조건) 정의를 포함하고 있으며, 결정된 검출한계가 어떻게 추정되었는지에 대한 설명을 포함하여야 함. 수학적 정의 또는 통계로부터 도출된 검출한계 추정치는 목표로 하는 검출수준에서 분석물질을 함유하는 시료를 분석함으로써 검증되어야 함. |
|
Ruggedness (둔감도) |
둔감도는 시험과정 중 작은변화에 영향을 받지 않고 분석물질의 농도를 결정할 수 있는 능력을 나타냄. 둔감도는 시험이 진행되는 과정 중 환경변화가 있을 때 이를 방지할 수 있는 실험계획을 포함해야 함. 다른 실험실에서 발생할 수 있는 예상되는 합리적인 변화를 반영하여 함. |
|
Interlaboratory study (시험실 간 교차시험) |
실험실 간 교차시험은 동일 분석방법을 다른 실험실에서 사용하기 위해 실제 시험에 사용될 수 있는지 여부를 결정하기 위하여 실시 함. 시험실 간 시험계획 및 결과는 방법검증 보고서에 포함되어야 함. 또한 실험실 간 연구로 인한 방법변경 사항에 대한 세부사항과 그 이유에 대한 설명이 포함 된 검토과정이 포함되어야 함. |
3.2.2. NATA [5]
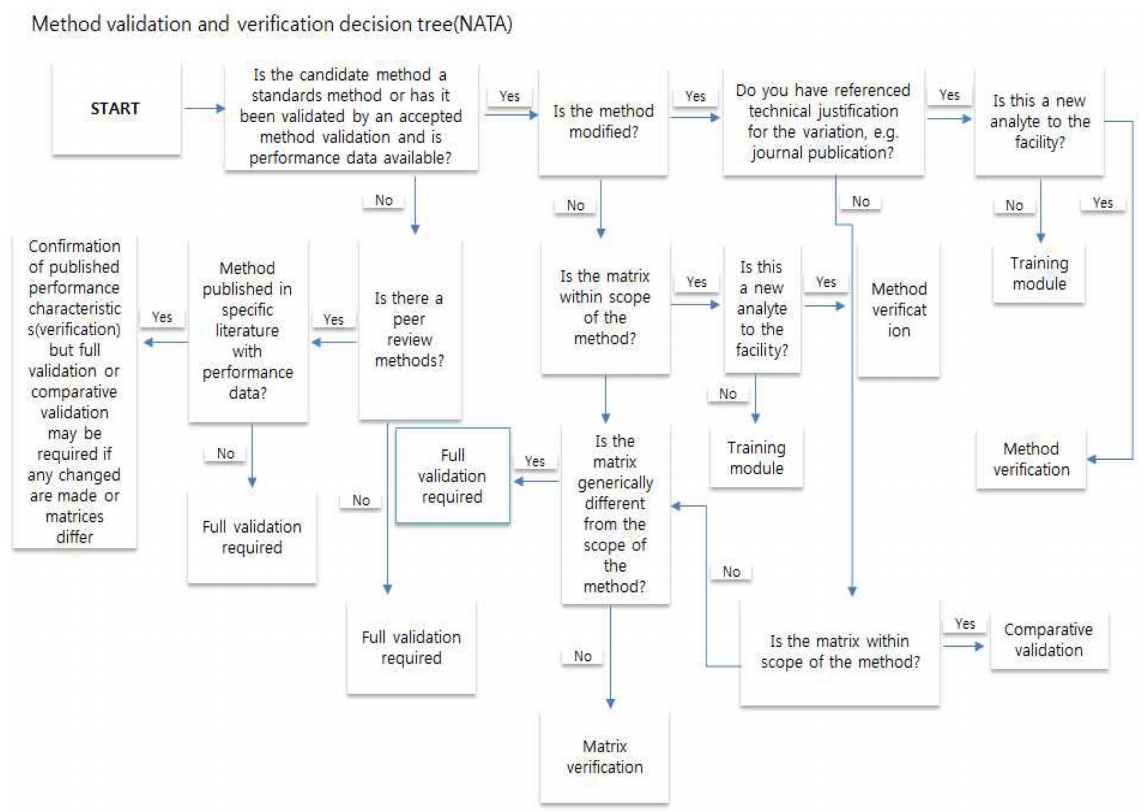
호주의 NATA는 시험기관에서 운영하고 있는 시험·검사 방법의 유효성 확인 과정에서 운영하고 있는 이화학적 시험방법의 검증 가이드라인을 지침으로 운영하고 있다. 이 지침에서는 시험방법의 유효성 확인과 관련된 플로우 챠트를 제시하여 매 과정마다 검토해야 되는 중요한 확인사항을 제시하고 있다. NATA에서 제시하고 있는 시험방법의 유효성 검증이 필요한 경우는 ① 새로운 후보 시험방법의 검토 ② 기존의 유효성 확인 단체에서 검증한 방법의 유효성 확인 ③ 데이터의 품질 검토 등 이러한 과정들을 필요로 할 때로 제안하고 있으며, NATA지침의 중요한 절차중의 하나는 매트릭스 검증과정을 별도로 추가하고 있다는 점이다. NATA에서 시험·검사방법의 유효성 검증과정은 크게 투 트랙(two track) 방식으로 적용하고 있으며. 정량시험방법의 유효성 검증과 정성시험방법의 유효성 검증으로 구분하여 각각 필요한 인자들을 제시하고 있다. 정량시험방법의 유효성 검증 인자로는 검출한계(Limit of Detection), 감도(Sensitivity), 선택성(Selectivity), 검량선의 직선성(Linearity of Calibration), 측정범위(Measuring Interval), 매질효과(Matrix effect), 진도(Trueness, bias), 정밀도(Precision), 정확도(Accuracy), 둔감도(Ruggedness), 측정불확도(Measuring Uncertainty)등을 제시하고 있다. 정성시험방법의 유효성 검증 인자로서는 감도(Sensitivity), 선택성(Selectivity), 검량선의 직선성(Linearity of Calibration), 매질효과(Matrix effect), 진도(Trueness, bias), 정밀도(Precision), 정확도(Accuracy), 둔감도(Ruggedness) 등을 제시하고 있다.
Fig. 4.
Data verification and data validation processes (NATA).
3.2.3. UKAS [6]
영국의 UKAS는 시험·검사방법의 유효성검증은 ISO/IEC 17025의 지침을 따르고 있다. 이 지침에서는 ① 비표준화 시험방법을 적용할 때, ② 시험실에서 자체 개발한 시험방법을 적용할 때 ③ 표준화된 시험방법을 다른 용도로 사용할 때 ④ 시험자가 기존의 표준시험방법을 다른 용도(확장 또는 수정)로 사용한 경우에 유효성확인 과정을 거치도록 하고 있다. 시험방범의 유효성 확인은 의도한 응용분야나 적용분야에 필요로 하는 목적을 충족하도록 확정된 범위로 하도록 하고 있다. 유효성확인 과정을 수행하는 시험실에서는 유효성 확인 과정의 결과물들, 유효성확인 과정, 의도된 목적대로 수행되었는지 여부 등에 대한 내용들을 기록하도록 하고 있다. 유효성 확인과정에서 적용하는 파라미터들은 측정 불확도, 검출한계, 방법의 선택성, 직선성, 반복성 또는 재현성, 강건성, 감도 등을 제시하고 있으며 적용하는 인자들은 고객들의 요구사항에 부합하도록 하고 있다.
3.2.4 Eurachem [7]
Eurachem에서는 시험방법의 유효성 검증을 필요로 하는 과정은 다음과 같이 정하고 있다 ; ① 특수한 문제의 발생으로 새로운 시험방법을 개발할 때 ② 개선을 필요로 하거나 또는 새로운 문제의 발생이 예측되는 경우 ③ 시간의 경과에 따라서 기존의 시험방법에 대한 신뢰도 평가가 필요할 때 ④ 기존의 시험방법을 서로 다른 시험실, 다른 분석자, 다른 장비 등을 사용할 때 ⑤ 새로운 시험방법과 기존에 사용하는 시험방법에 대한 동등성의 입증이 필요로 할 때로 정의하고 있다. Eurachem에서 적용하고 있는 유효성 검증은 성상확인시험(Identification test), 불순물에 대한 정량시험(Quantitative test for impurity), 목적성분에 대한 정량시험(Quantification of component)로 분류하고 있다. 이 과정에서 적용하는 파라미터들은 선택성(Selectivity), 검출한계(Limit of detection), 정량한계(Limit of quantification), 범위(Working range, linearity), 진도 (Trueness, Bias), 정밀도(Precision) 등이다.
Fig. 5.
Method validation processes of UKAS.
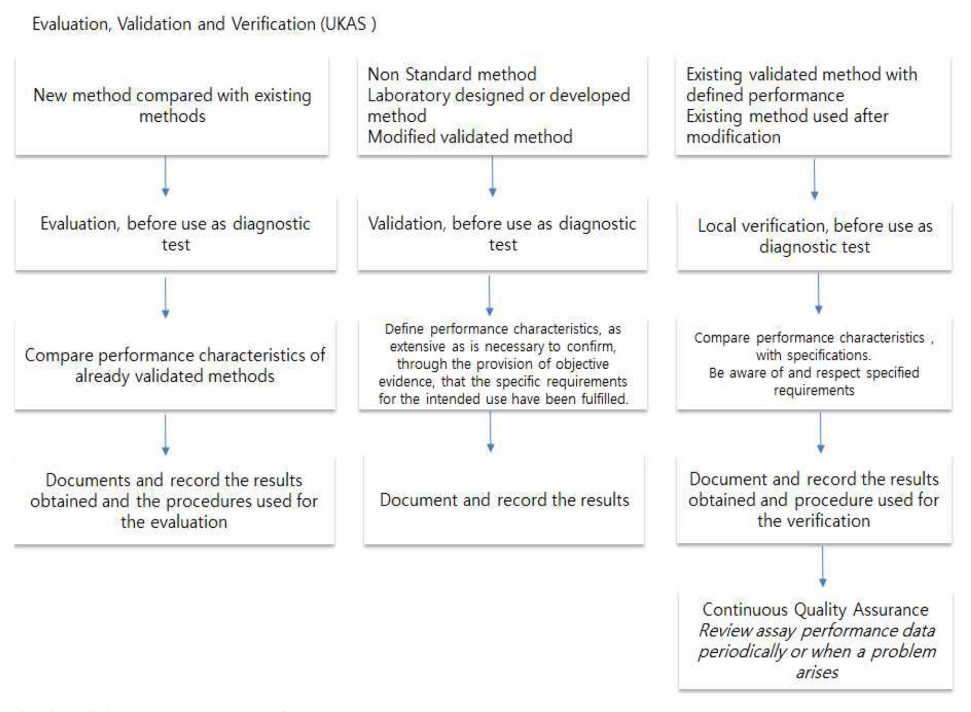
Fig. 6.
The method validation processes of Eurachem.
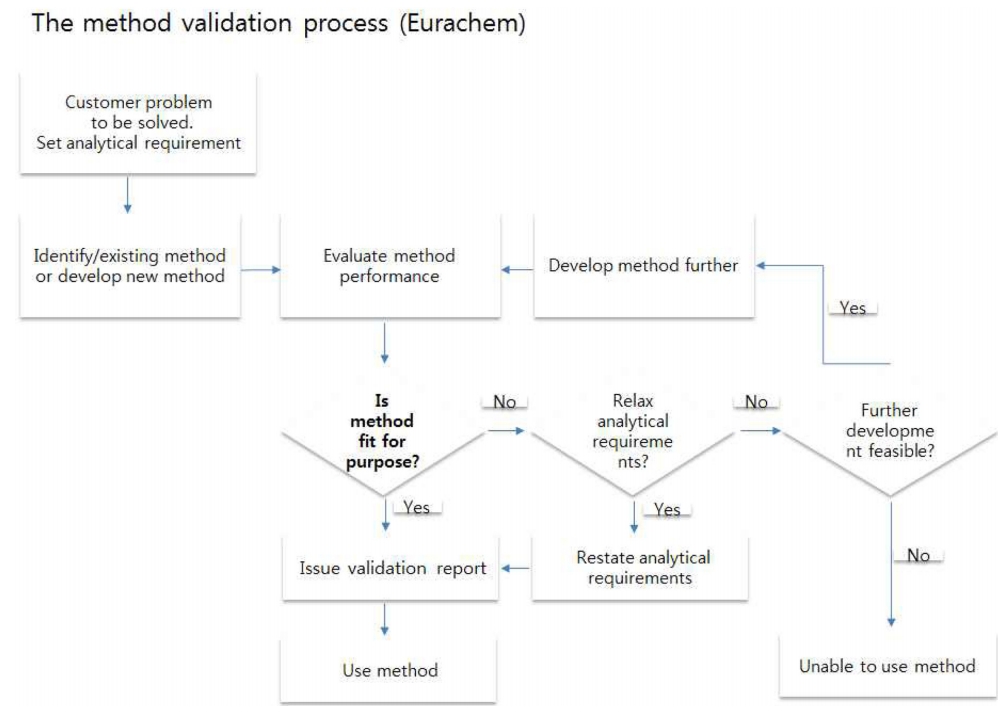
Table 6.
Definitions of method validation parameters and extent of validation works by NATA
|
Parameter (주요인자) |
용어정의 또는 설명 |
|
Range (범위) |
분석 절차의 교정의 선형성은 주어진 분석 매개 변수의 농도에 비례하는 신호(반응값)를 생산할 수 있는 능력임. |
|
직선성의 결정은 검정 방정식(calibration equation)에 적용되므로 기기측정 만 포함됨. 다음사항을 포함해야 함. |
|
- 6개 이상의 검정을 위한 표준 (농도가 0에 가까운 빈도 또는 교정표준을 포함)이 있어야 함. |
|
- 표준용액의 농도범위는 균등하게 배치(조제)되어야 함. |
|
- 농도범위는 0~150% 또는 50~150%를 포함해야 함. |
|
- 2회~3회 이상 반복 측정되어야 함. |
|
Measuring Interval (검량선 농도 간격) |
검량선 농도간격은 일반적으로 선형성(직선성)에 대한 검토를 필요로 하며, 유효성 확인과정의 정밀도, 정확도 및 직선성이 유효함을 입증한 분석물질(RM)을 분석하기 위한 상한 및 하한농도 사이의 농도간격으로 정의됨. |
|
Matrix effect (매질효과) |
유효한 측정 농도범위를 결정하기 위하여 분석물질의 회수율에 대한 매트릭스 영향을 평가해야함. 일반적으로 시료에는 분석대상물질 뿐만 아니라 추가적인 성분(방해물질)도 포함해야 함. |
|
Selectivity (선택성) |
분석대상 물질을 선택적으로 측정하는 것이 중요하며, 선택성은 분석물질과 상대되는 불순물(방해물질), 분해생성물 및 매트릭스 성분과 같은 간섭물질 존재하에서 분석물질을 선택적으로 분석하는 능력임. |
|
Sensitivity (감도) |
감도는 분석물질의 농도의 변화에 따른 측정된 반응 함수값(흡광도, 피크면적 등)의 변화율을 말함. 감도가 높을수록 일반적으로 동적범위는 작아짐. 감도는 시험실 분석환경의 지속적인 품질보증절차의 일부로서 점검되어야 함. |
|
Accuracy (정확도) |
단일 측정물질에 대한 특성이며 무작위(random) 및 체계적인(systematic) 오류의 영향을 받음. 측정결과의 정확도는 결과가 실제 값에 얼마나 가까운지를 나타내므로 정밀도와 진도(바이어스(bias)로 표현됨)의 효과가 모두 포함됨. 체계적 오류를 제거하면 정확도가 향상되지만 정밀도는 변하지 않을 수도 있음. 정확도 평가는 '목적의 적합성'에 달려 있으므로 정확성과 정확성을 검증기준에 따라 평가해야 함. |
|
Trueness (진도)/bias (편향) |
진도(또는 편향)은 무한 수의 반복 측정된 양 값과 참조 농도(량)값과의 평균의 일치도를 나타냄. 무한 수의 반복 측정된 양 값과 참조 수량 값의 평균 간의 일치도를 나타 냄. |
|
Limit of detection (검출한계)/Limit of quanitation (정량한계) |
검출한계(LOD) 또는 정량한계 (LOQ)의 결정은 일반적으로 0에 가까운 농도(낮은 수준 농도)를 검출할 수 있는 능력을 나타냄. LOQ값 보다 큰 분석물질의 농도를 측정하기 위해 적용될 방법에 대해서는 LOD 또는 LOQ를 추정할 필요는 없으나, 보고된 분석결과의 평가에 영향을 미칠 수 있음. |
|
Precision (정밀도) |
정밀도는 일반적으로 표준편차 또는 상대표준 편차와 같은 수치로 표현됨. 목표로 하는 정밀도가 정상 작동조건에서 적용한 시험방법의 성능을 정확하게 반영하려면 주어진 조건에서 결정되어야 함. |
|
Ruggedness (완건성, 견고성) |
방법의 견고성(완건성)은 분석결과가 온도, pH, 시약 농도, 추출시간 등의 작은 변화와 같이 방법에 기술된 실험조건이 사소한 변화에 영향을 받지 않는 정도를 나타냄. 견고성 테스트는 정상적인 시험과정 중의 신뢰도를 나타내는 것으로서, 측정(또는 분석과정)이 시험자 또는 시험실의 변경에 의한 시험결과의 변동요인을 확인하는 데 사용함. |
|
Measuring Uncertainty (측정불확도) |
측정불확도(MU)는 충분한 통계적인 근거자료가 있는 경우는 측정결과와 직접 관련된 중요한 매개변수로 정의됨. 이는 측정량(농도)에 합리적으로 영향을 미치는 전체적인 영향을 확인할 수 있는 평가요소로 볼 수 있음. |
Table 7.
UKAS policy on the participation in proficiency testing
|
Parameter (주요인자) |
용어정의 또는 설명 |
|
Introduction (개요) |
ISO/IEC 17025는 실험실이 수행된 시험 및 교정의 유효성을 평가하기 위한 품질관리 절차를 요구하고 있음. 모니터링은 시험소 간 비교 또는 숙련도 시험 프로그램에 참여하는 것을 포함할 수 있으며, 다른 방법을 통한 반복적인 시험/교정을 포함하도록 권장하고 있음. |
|
Scope (범위) |
지침에 따른 정의는 실험실을 포함한 인증을 받은 시험실 또는 받으려는 시험실 시험분석자들이 해당 시험과정을 수행할 때 준수하도록 하고 있음. |
|
Terminology (용어) |
숙련도시험(PT)은 시험소 간 비교를 통해 사전 설정된 기준에 대한 시험기관의 교정, 시험성능 또는 검사기관에 대하여 시험실간의 비교를 통하여 검정능력과 시험능력에 대한 결정 하도록 하고 있음. |
|
Policy (정책) |
공인된 모든 시험실은 공인된 시험실이 숙련도시험에 참여할 수 있도록 하는 것이 UKAS의 정책임. 달성하고자 하는 목적을 위해 시험실간 비교에 성공적으로 참여함으로써 다음 사항을 입증 받도록 하고 있음. |
|
- 방법의 성능특성에 대한 평가. |
|
- 참조자료의 특성에 대한 기술. |
|
- 두 개 이상의 시험실결과에 대한 자체적인 비교. |
|
다른 유형의 QA 참여시 참고사항 |
실험실과 검사기관들은 다른 QA(Quality Assurance)조치(특히 폐쇄, 정량, 정량화된 농도에 대한 편향)를 면밀히 분석한 후 참여수준과 빈도를 결정하도록 하고 있음. |
|
- 참조물질들 정기적인 사용 |
|
- 독립적인 기술들을 활용한 분석 비교 |
|
- 방법개발, 검증, 표준물질 특성화 연구 참여 |
|
- 내부품질 관리 수단 사용 |
|
- 기타 시험실간/시험실내 비교, 예를 들면 시험실내에서 블라인드샘플 분석 |
Table 8.
Extent of validation work for four types of analytical applications by Eurachem
|
Performance characteristics |
Types of analytical application
|
|
Identification test |
Quantitative test for impurity |
Limit test for impurity |
Quantification of main component |
|
선택성(Selectivity) |
x |
x |
x |
x |
|
검출한계(Limit of detection) |
|
|
x |
|
|
정량한계(Limit of quantification) |
|
x |
|
|
|
Working range including linearity |
|
x |
|
x |
|
Trueness (bias) |
|
x |
|
x |
|
Precision (repeatability and intermediate precision) |
|
x |
|
x |
3.2.5. IUPAC [8]
IUPAC은 시험방법의 유효성검증과 관련된 적용인자들로서 시험·검사기관에서 적용하고 있는 파라미터들보다 더 많은 유효성 검증인자들을 적용하고 있다. 적용하고 있는 인자들로서는 적용성, 선택성, 검량선의 직선성, 진도, 정밀도, 회수율, 범위, 검출한계, 정량한계, 감도, 둔감도, 목적의 부합성(Fitness for purpose), 매트릭스 변동성(Matrix Variation), 측정불확도 등을 제시하고 있다. 검량선의 직선성(Calibration and Linearity)을 확인하는 추가적인 인자로는 검량성기울기 및 잔차(Linearity and Intercept), 매트릭스 평가(Test for general matrix effect), 검량선 작성절차(Final calibration procedures)를 제시하고 있으며, 진도에 대한 추가적인 확인방법으로는 CRM(certified reference material), RM(reference material), Reference Method를 추가적으로 제시하고 있다.
Fig. 7.
Method validation processes of IUPAC.

Table 9.
Definitions of parameters and extent of validation works by Eurachem
|
Parameter (주요인자) |
용어정의 또는 설명 |
|
Selectivity (선택성) |
특정한 간섭에 의해서 분석시료(매트릭스 포함)중에 존재할 것으로 예상(목표)되는 물질을 선택적으로 측정하는 능력으로 정의됨. 간섭이 존재하는 경우 시험방법의 선택성은 다른 시험방법과 비교하여 분석물질을 반복 측정함으로서 나타낼 수 있음. |
|
Limit of detection (검출한계) |
LOD는 여러 가지 표현으로 표현됨(Limit of Detection, Minimum Detectable Value, Detection Limit). “0”로부터 의미 있는 분석물질의 농도를 말하며, 특정한 신뢰도를 갖는 방법으로 검출 가능한 가장 낮은 농도로 정의됨. |
|
Limit of Quantification (정량한계) |
LOQ는 적용 가능한 분석능력으로 결정될 수 있는 가장 낮은 수준의 농도로 정의됨. 실질적으로 LOQ는 얻을 수 있는 가장 낮은 수준의 표준편차에 팩터(kq)값을 곱하여 계산하며, IUPAC에서 팩터(kq)값은 10을 제안하고 있음. |
|
Working Range (범위) |
적용범위는 적용한 시험방법이 분석결과가 허용할 수 있는 오차범위를 제공할 수 있는 검량선의 간격으로 정의됨. 작업범위를 평가하기 위해서는 1) 기지농도의 시료와 공시험용액 2) 측정의 모든 과정을 통해 사용된 전체시료 3) 의도한 분석범위를 커버할 수 있는 다른 농도의 시료들 4) 분석과정에 사용된 시험장비가 필요함. |
|
Trueness (진도) |
시험방법으로 얻은 분석결과의 질을 나타내기 위한 성능 특성의 평가는 진도, 정밀도 및 불확도를 사용함. 현재도 다른 개념의 에러(Random, Systematic and Gross errors), 정확도와 관련된 인자(Trueness and Precision) 및 불확도 등을 진도의 종합적인 평가인자로 활용하고 있음. |
|
Precision (정밀도) |
정밀도는 시험결과 값들 간의 근접정도를 나타내는 인자임. 정밀도는 분석결과들의 퍼짐정도(상대표준편차), 특정한 조건하에서 반복측정에 대한 결과들로부터 계산되며, 정밀도는 측정값의 반복성(Measurement Repeatability) 및 측정의 재현성(Measurement Reproducibility)를 나타냄. |
|
Measurement Uncertainty (측정불확도) |
측정불확도란 측정된 분석결과들이 목표로 하는 측정값에 대하여 표현 가능한‘간격(interval)’로 정의됨. 불확도 평가는 결과에 영향을 미치는 모든 가능한 영향들을 고려하여 평가하여야 함. |
|
Ruggedness (둔감도) |
시험조건의 작은변화 또는 고의적인 임의 변화에 영향을 받지 않고 견딜 수 있는 능력을 평가하는 인자임. 둔감도는 시험방법의 적용과정에서 방법에 대한 신뢰성 평가 인자로 활용됨. |
4. 결 론
국내·외 시험검사기관에서 적용하고 있는 시험방법의 유효성검증 과정은 지침 또는 가이드라인에서 제시하고 있다. 유효성 검증과정에서 적용하고 있는 파라미터들은 특이성, 선택성, 직선성, 감도, 정확도, 정밀도, 진도, 검출한계, 정량한계, 범위, 완건성, 둔감도, 측정불확도 등을 공통적으로 조사되었다. 시험·검사기관에서 실시하는 시험방법의 유효성 확인은 신규 시험방법의 확인, 비표준화 시험방법과 표준화된 방법 간의 비교, 확장이 필요한 시험방법에 대한 확인, 다른 시험기관 또는 다른 분석자간의 적용한 시험방법의 검증, 시험방법간의 유사성 증명이 필요한 경우, 기존에 검증된 시험방법의 재검증이 필요한 경우에 적용하는 것으로 나타났다. 본 연구결과에서 조사된 유효성 검증과정의 파라미터들은 향후 환경분야 시험·검사방법 등에 대한 유효성확인 지침 마련 시 충분히 활용이 가능할 것으로 판단되었다.
Table 10.
Definitions of parameters and extent of validation works by IUPAC
|
Parameter (주요인자) |
용어정의 또는 설명 |
|
Applicability (응용범위) |
유효성 검증문서에서는 각각의 인자에 대한 평가 후 다음과 같은 정보들을 제공하여야 함. |
|
- 분석물질(목적하고자 하는)의 종류 |
|
- 정량범위 내에서의 물질의 예측 가능한 농도 |
|
- 유효과정에 포함된 구체적인 분석물질 |
|
- 시험분석과정에 사용되는 분석장비 및 시약 |
|
- 검정곡선 |
|
- 시험자의 안전보호 조치 등이 검토되어야 함. |
|
Selectivity (선택성) |
간섭물질이 존재할 때 정확하게 분석할 수 있는 정도로 정의되며, 선택성은 존재할 수 있 는 중요한 간섭물질에 대해 평가되어야 함. 화학적인 원리에 의해 시험에 반응할 가능성이 있는 간섭물질을 확인하는 것이 중요함. |
|
Calibration and linearity (검정 및 직선성) |
분석과정의 전체적인 큰 오류를 제외하면 교정 가능한 오류는 대개 사소한 원인으로 발생 하며, 보정이 가능한 무작위적인 오류는 전체적으로 평가가 가능한 바이어스(bias)의 일부로 볼 수 있음. 유효성검사는 검정과정이 (a) 선형적이고 (b) 원점을 통과하는지, (c) 시험재료 의 매트릭스에 영향을 받는지 여부 등을 고려해야 함. |
|
Trueness (진도) |
진도는 "바이어스(bias)"측면에서 정량적으로 표현됨. 바이어스는 일반적으로 방법의 응답을 기준과 비교하여 결정되며, 기준값의 불확도가 무시할 수 없는 경우는 표준물질의 불확실 성과 통계과정의 변동성을 고려해야 함. |
|
Precision (정밀도) |
정밀도는 규정된 조건 하에서 얻은 독립적인 테스트 결과 간의 일치하는 정도로 정의되며, 표준편차 또는 상대 표준 편차로 표현됨. 정밀도와 바이어스(bias)의 차이는 시험실 전체적 인 분석 시스템의 차이를 나타낼 수 있음. |
|
Recovery (회수율) |
회수율은 유효성확인 과정에서 정의한 허용범위와 반드시 동일하지 않을 수 있음을 인식하 는 것이 중요하며, 검정이 넓은 농도범위를 포함할 수 있지만, 회수율 평가를 통한 유효성 확인은 제한된 범위를 나타낼 수도 있음. |
|
Range (범위) |
분석결과가 신뢰성을 확보했다고 판단되는 분석물질(의도했던)을 분석하기 위하여 검량선 작성에 필요한 표준물질의 농도간격으로 정의되며, 범위는 목표로 하는 검출농도와 반드시 일치할 필요는 없음. |
|
Detection Limit (검출한계) |
넓은 의미에서 검출한계는 분석물질의 최소량 또는 농도임. 시험방법 개발에서 추정된 검 출한계는 완전한 분석방법을 특성화(정규화)하기 위해 사용된 것과 개념적인 측면적용한 시 험방법과 동일하지 않을 수 있음을 인식해야 함. |
|
Limit of determination (검출한계)/Limit of quantification (정량한계) |
분석방법이 작동할 수 없는 농도 이하를 명시하는 것이 유용하며, 그 정밀도는 임의로 10% RSD로 정의됨. 임의로 검출한계의 고정배수를 사용할 수도 있음. 농도의 함수로서 측정불확도로 표현하려고 시도하는 것도 바람직 함. |
|
Sensitivity (감도) |
방법의 민감도는 검정곡성의 기울기로 정의됨. 분석장비의 선택에 따라서 임의적으로 편차가 클 수 있음. 결과값의 신뢰도 확보과정에서는 분석장비가 일관성 있는 분석결과를 생산했는지 비교할 수 있음. |
|
Ruggedness (둔감도) |
둔감도는 적용한 분석방법의 적용과정의 변화에 대한 분석결과의 저항수준을 평가하는 척 도임. 이를 위해서 실험 파라미터의 한계를 분석방법을 정한 프로토콜에서 규정되어야 함. 분석결과에 영향을 줄 수 있는 방법의 측면을 식별하고 견고성 있는 평가방법을 사용하는 것이 이상적임. |
|
Fitness for purpose (목적의 부합성) |
부합성은 분석자와 데이터의 최종 사용자간에 합의 된 요구를 설명하는 기준과 일치하는지 여부를 판단하는 것으로 평가될 수 있음. 데이터의 오류는 목표로 하는 시험결과 값보다 더 높은 빈도의 오류를 발생 시키는 수준이 되어서는 않됨. |
|
Measurement Uncertainty (측정 불확도) |
측정불확도는 분석의 전과정을 포괄적으로 포함한 모든 종류의 무작위 오류에 대한 적절한 허용치를 고려한 중대한 영향을 포함한 분석결과에 대한 평가인자임. |
감사의 글
연구는 국립환경과학원 환경분야 시험검사 방법의 유효성 검증 기법 연구사업(과제번호: NIER-RP2018-146)으로 수행되었으며, 연구진들은 국립환경과학원의 지원에 깊은 감사를 드립니다.
Table 3.
Summary of validation parameters used by the Ministry of Food and Drug Safety [
3]
|
구분 |
주요내용 |
|
적용범위 |
1) 식품 중 일반성분 및 영양성분에 대한 확인시험, 함량 등에 대한 시험법 |
|
2) 식품 중 식품첨가물 및 기구·용기·포장에 대한 시험법 |
|
3) 미생물 관련 시험법 |
|
4) 식품 중 농약 및 동물용의약품에 대한 확인시험, 잔류량 등에 대한 시험법 |
|
5) 건강기능식품 등에 대한 확인시험, 함량 또는 역가 관련 시험법 |
|
6) 식품 중 자연독소, 중금속 및 방사능 등 유해물질에 대한 확인시험, 함량 등에 대한 시험법 |
|
7) 유전자변형식품에 대한 시험법 |
|
8) 기타 식품 기준·규격 및 안전관리에 관한 시험법 등 |
|
주요인자 |
선택성(Selectivity), 정밀도(Precision), 반복성(Repeatability), 재현성(Reproducibility), 검출한계(Limit of Detection, LOD), 정량한계(Limit of Quantification, LOQ), 민감도(Sensitivity), 직선성(Linearity), 적용범위(Working Range), 인증표준물질(Certified Reference Material, CRM), 실험실내 검증(Intralaboratory Validation), 실험실간 검증(Inter-laboratory Validation) |
Table 4.
Definitions of method validation parameters used by the Ministry of Food and Drug Safety
|
Parameter (주요인자) |
용어정의 또는 설명 |
|
선택성 (Selectivity) |
시험법의 선택성은 간섭물질이 존재할 때의 측정의 정확도를 뜻한다. 크로마토그래피/질량 분석 등의 분석방법은 선택성이 매우 높아질 수 있으며, 잠재적인 간섭물질의 영향은 의심되는 간섭물질을 사전에 정해진 농도만큼 첨가한 시료를 분석하여 확인할 수 있음. |
|
정확도 (Accuracy) |
정확도는 시험결과의 품질을 측정하는 것으로 시험결과인 측정값이 표준값(Accepted Reference Value)에 대해 얼마나 근접하는가에 대한 것임. 정확도는 일반적으로 분석회수율(Analytical Recovery) 결과로 판단함. |
|
정밀도 (Precision) |
시험법의 정밀도는 지정된 조건 하에서 시행된 각각의 반복적인 시험결과들 간의 근접한 정도(분산정도)를 나타내는 것. 정밀도는 일반적으로 반복된 결과의 표준편차(Standard Deviation, SD) 또는 상대표준편차(Relative Standard Deviation, RSD)로 나타냄. |
|
검출한계 및 정량한계 (Limit of detection and limit of quantitation) |
시험법의 검출한계는 0과는 확실하게 구분할 수 있는 분석 대상물질의 최소량 또는 최저 농도이며, 시험법의 정량한계는 보통 ‘적절한 불확도 수준으로 결정 가능한 분석 대상물질의 최저 농도’로 정의함. |
|
민감도 (sensitivity) |
시험법의 감도는 분석 대상물질의 농도(양)의 변화에 따른 측정값의 변화에 대한 비율이다. 시험법의 감도(검량선의 기울기)가 클수록 분석 대상물질 농도의 미세한 변화를 확인하기가 더 용이함. |
|
직선성 (Linearity) |
시험법 검증 과정의 일부로서 검정모델(Calibration Model)의 유효성을 수립할 때는 다음의 규칙을 활용할 것이 권장된다. |
|
가) 검정 표준은 최소 5개 농도 이상이어야 한다. |
|
나) 검정 표준은 측정하고자 하는 농도 범위에 고르게 분포하고 독립적으로 만들어져야 한다. |
|
다) 검정 표준의 농도범위는 발생 가능한 농도의 0~150% 또는 50~150% 중 더 적절한 범위가 포함되어야 한다. |
참고문헌
1. ISO/IEC 17025:2005 General requirements for the competence of testing and calibration laboratories
2. KOLAS, 화학적 시험방법의 유효성 확인을 위한 지침, 2012.
3. 식품의약품안전청, "의약품등 시험방법 검증 가이드라인 적용을 위한 해설서", 2012.
4. EPA, Guidance on Environmental Data Verification and Data Validation, 2002.
5. NATA, Guidelines for the validation and verification of quantitative and qualitative test methods, 2013.
6. UK standards for microbiology investigations, issued by the standards unit, Microbiology Services, PHE, 2011
7. Eurachem, the Fitness for Purpose of Analytical Methods - A Laboratory Guide to Method Validation and Related Topics, 2nd edition. 2014.















