대청호 유입 소하천 유기물질 유출 특성
Characteristics of Organic Matters in Small Streams into the Daecheong Reservoir
Article information
Trans Abstract
While BOD5 has been improved in Korea's major rivers and reservoirs over the last 10 years, CODMn is still on the rise. The purpose of this study was to investigate the leakage characteristics of refractory organic oatter (ROM) in Juwon stream and Pumgok stream flowing into Daecheong Reservoir, the most important drinking water source of Geum River basin. ROM was extracted with hydrophilic (Hi) and hydrophobic (Ho) organics using the XAD resin method. XAD analysis showed that hydrophobic ratios were 52.1–77.1 % and 52.7-97.1 % of dissolved organic carbon (DOC), respectively, in the Juwon and Pumgok streams. Hydrophobic organic matters were classified as humic substances originating from forest areas upstream of the watershed. In addition, the Ho/Hi ratio increased during the rainfall period (seven–nine months) and decreased during the nonrain period, and the Ho component, including hydrophobic acid (HoA) during rainfall, was the main component flowing into Daecheong Reservoir through the runoff. Total organic carbon (TOC) and COD showed a strong positive correlation between organics to confirm the association between ROMs. The results of this study confirmed the characteristics and background concentrations of the ROMs of some tributaries into the Daecheong Reservoir. In the future, continuous investigation and research will be needed to manage the natural organic matter of the main stream of Geum-river, including Daecheong Reservoir.
1. 서 론
물 환경 중 과다하게 존재하는 유기물질은 수생 생물의 먹이로 이용되어 미생물의 급속한 증식, 용존산소의 과다한 소비를 일으키고 결국 수질오염을 유발하게 된다. 이에 수질 관리 차원에서 오염도 평가를 위한 주요 지표로 수중 유기물을 평가하고 있다[1,2]. 이러한 유기물질은 미생물에 의한 분해 가능 여부에 따라 생물화학적 산소요구량(BOD, Biochemical Oxygen Demand) 농도로 대표되는 생분해성 유기물질과 난분해성 유기물질로 나뉘며, 대표적인 난분해성 유기물질의 지표로는 화학적 산소요구량(COD, Chemical Oxygen Demand)과 총유기탄소(TOC, Total Organic Carbon)가 활용되고 있다. 그동안 BOD를 지표항목으로 하는 수질 개선 노력으로 지표수 중 생분해성 유기물질은 어느 정도 감소 및 유지 되어 왔으나 COD, TOC는 증가 추세인 것으로 조사되어, 난분해성 유기물질에 대한 관리 및 필요성이 제기되고 있다[3]. 이러한 난분해성 유기물질이 수계 내 존재하는 경우 상수처리 효율성과 염소소독부산물(DBPs, disinfection byproducts)의 생성에 영향을 미치며[4], 수계 내 생태계 교란, 정수처리 공정에서 인체 유해한 THM 생성 등의 문제점이 있는 것으로 조사된 바 있다[5-9]. 지표수 중 난분해성 유기물질의 유입 경로는 크게 외부유입과 생태계 내 생산(조류증식)에 따른 내부생성 요인으로 나뉠 수 있다[10]. 외부 유입의 경우 유역의 산림 및 토지 이용도와 관련이 깊은 비점오염원을 통해 주로 유입되는 것으로 알려져 있다[11,12]. 현재 환경부는 이러한 난분해성 유기물질의 농도를 반영할 수 있도록 수중 유기물질 관리 목표를 BOD에서 TOC로 전환하고, 공공수역 내 유기물질 저감 목표 달성을 위한 계획을 진행하고 있다[13]. 수계 중 난분해성 유기물질에 관한 연구로는 현재까지 국내 주요 수계에서 유기물 수지 분획과 SUVA(Specific Ultra-violet Absorbance, 고유흡광도) 방법으로 주요 저수지 및 일부 지점에 대해 조사된 바 있다[14-16]. 국외에서도 유기물 기원 추적에 사용하는 EEM(Excitation Emission Matrix,형광측정법), 유기물 분자량의 분포와 구조 및 기원을 파악하는 SEC-OCD(Size Exclusive ChromatographyOrganic Carbon Detection)등 다양한 방법으로 연구된 바 있다[17-20]. 우리나라는 국토면적 중 산림이 64%로 가장 큰 비율을 차지하고 있다. 특히 금강의 주요 취수원으로 사용되는 대청호의 토지이용도는 70%이상이 산림이나[21] 이러한 산림에서 유래하는 난분해성 유기물질에 대한 연구는 부족한 상황이다.
따라서, 본 연구에서는 금강유역의 주요 호소인 대청호를 대상으로 산림에서 유래한 난분해성 유기물질의 유출 특성을 조사하고 각 유기물 지표 항목간의 상관성 분석을 통해 난분해성 유기물질의 유출 특성을 가장 잘 대표하는 항목을 찾아 향후 유기물 관리에 이용하도록 제시하고자 한다.
2. 재료 및 방법
2.1. 대상유역 선정 및 자료분석
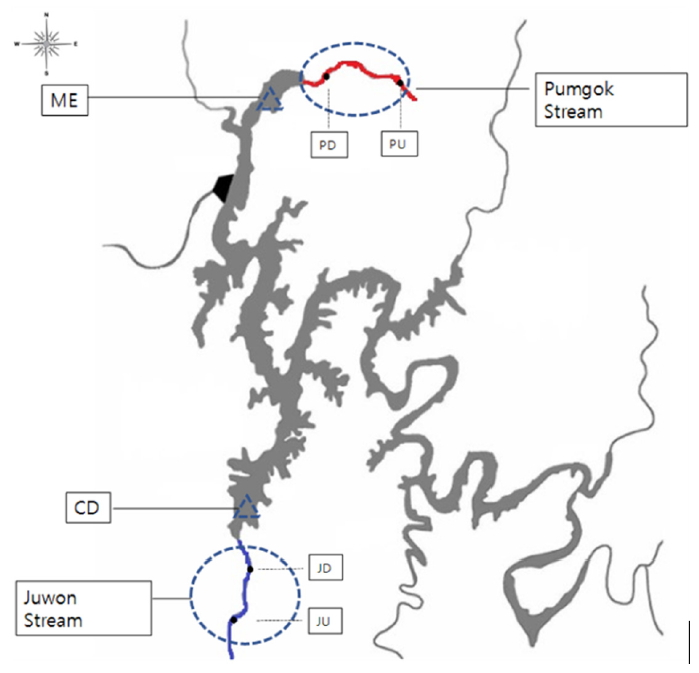
연구 대상 지점은 Fig. 1과 같이 대청호로 유입하는 하천 중 난분해성 물질의 유출 특성 분석을 위해 주원천 품곡천과 대청호를 대상으로 주원천 품곡천 상하류 각1개 지점 대청호내(추동, 문의) 2개 지점을 선정하였다. 추동은 상류에서 주원천, 문의는 상류 품곡천이 유입되는 각각의 취수 지점에 해당된다. 조사지점의 유역 면적은 주원천 7.7 km2으로 토지이용현황은 산림지역이 84%로 가장 많이 분포하고 있으며, 다음으로 농업지역(5.2%), 초지(4.9%), 시가화(3.4%)순이며, 품곡천은 9.3 km2로 산림(68.4%), 농업(28.4%), 초지(5.8%), 시가화(2.7%)순으로 분포하고 있다[22].
지점의 시료채취는 2016년 2월부터 12월까지 주1회씩 총 41회 모니터링을 실시하였다. 강우량은 기상청에서 제공하는 실시간 자료를 이용하였고, 수질항목은 생물화학적 산소요구량(BOD5), 화학적 산소요구량(CODMn), 총유기탄소(TOC)를 대상으로 시료를 4°C로 냉장 운반하여 수질오염 공정시험기준(2016)에 준하여 분석하였다.
2.2. 분석방법
2.2.1 유기물지표 분석방법
유기물 수질 오염지표는 BOD5, CODMn, TOC 등이 있다. BOD5는 하천수를 20°C에서 5일간 항온배양 후 수중에 있는 호기성 미생물의 증식과 호흡작용 등에 의해서 소비된 산소의 양을 통해 측정하였다. CODMn은 분석시간이 짧고 측정은 간단하나 산화율이 낮은 특성을 가지고 있다. 총유기탄소량인 TOC는 저농도에서도 재현성이 우수하며 오염물질 및 난분해성에 대한 대응이 높고[3] 분석시간이 짧다는 장점이 있다. 또한 다량의 시료 분석이 가능하고 자동화로 인해 인건비의 절감 효과가 있다. TOC 분석은 공정시험 기준에 제시된 전처리 방법에 준하여 시료의 균질화를 위해 초음파 파쇄와 체거름 과정을 거친 후 자체 자석 교반이 가능한 유기탄소분석기(Sievers 5310C, GE, USA)를 사용하였다. 용존형 유기탄소 DOC(Dissolved Organic Carbon)는 500°C에서 2시간 태운 GF/F여지(Whatman 0.7 µm)에 채취한 시료의 일정량을 여과시켜 용존성으로 분류한 후 TOC 분석기로 분석하였으며, 입자형 유기탄소 POC (Particulate Organic Carbon)는 TOC에서 DOC농도를 제외한 값을 계산하였다.
2.2.2. 난분해성유기물 분석
2.2.2.1 XAD resin분석
본 연구에서는 자연유기물질이 가지는 중요한 특성 중 하나인 친수성(Hydrophilic, Hi), 소수성(Hydrophobic, Ho)을 확인하기 위하여 XAD 수지 흡착법을 사용하여 난분해성 유기물을 분리 분석하였다(Table 1 및 Fig. 2). 소수성 물질은 humic 물질과 같은 방향족 물질의 우세함을 의미하기도 한다. 분리방법은 ⅰ)XAD resin에 0.1 M HCL, 1 M HCL, 1 M NaOH를 약 100 mL 흘려주어 각 컬럼의 resin을 전처리 한다. ⅱ)여과지(GF/F)로 여과한 용존유기물 시료(DOC1, 200 mL)를 진한 HCl를 이용하여 pH 2 이하로 조절하고 XAD 컬럼에 1.0~1.5 mL/min 유속으로 흘러 보내준다. 이 과정에서 컬럼을 통과하는 유출수 DOC2는 resin에 흡착되지 않은 친수성(Hi)에 해당된다. ⅲ)컬럼을 통과하지 못하고 resin에 흡착되어있는 시료는 0.1 N NaOH 50 mL를 컬럼의 역방향으로 통과시켜 resin에 흡착되어 있는 성분을 탈착시킨 후 나오는 물질은 소수성(Ho)으로 DOC3에 해당된다. 이상의 XAD resin 분리에 따른 DOC1, DOC2, DOC3를 분석하였다[23].
친수성 유기물 성분(Hi) = DOC2 − Blank2
소수성 유기물 성분(Ho) = DOC1 − (DOC2 − Blank2)
소수성 산 성분(HoA) = (DOC3 − Blank1) × (NaOH 탈착부피/시료 부피)
소수성 중성 성분(HoN) = Ho – HoA
2.2.2.2. EEM 형광분석
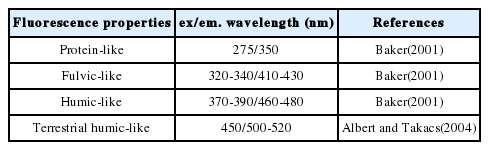
EEM 형광분석은 유기물의 기원을 추적할 수 있는 분석방법으로 수계내의 토지 이용도와 깊은 관련이 있다[24]. 대상 시료의 분석은 GF/F(Whatman, 0.7 µm) 여과지를 회화로 에서 3시간 동안 450°C로 회화한 후 여과한 시료를 석영셀을 이용하여 형광분광계(Cary Fluorescence spectrophotometer, Agilent Technologies, USA)로 분석하였다. 형광 EEM은 여기(Excitation) 및 방출(Emission)파장에서 형광세기 조절은 슬릿(Slit)폭을 10 nm간격으로 고정하여 측정하고, 여기파장의 형광광도 범위는 200~500 nm로 설정하고 방출파장의 형광광도 범위는 280~550 nm로 조절하여 시료를 측정하였다. 시료 내 자연유기물의 형광값은 시료의 형광 측정값에서 초순수의 형광측정 값을 차감하여 산출하였으며, 온도, 습도, 전원 등 외부환경 영향으로 인한 형광분광계 신호의 변동을 줄이기 위해 황산염을 0.05 N 황산용액에 녹여 여기파장 350 nm, 방출파장 450 nm에서 측정한 후 그 값을 이용하여 분석시료에서 얻어진 형광값을 나눈 값으로 형광세기 단위를 quinine sulfate equivalents (QSE)로 보정하였다.
3. 결과 및 고찰
3.1. 대청호 연간 수질현황
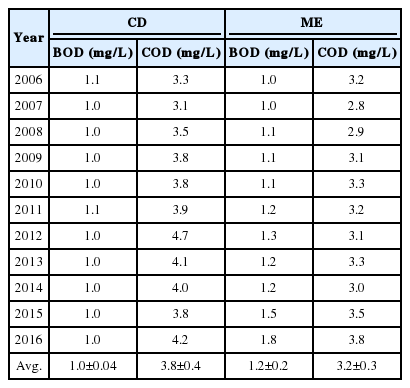
Table 2은 대청호의 취수지점인 추동(CD), 문의(ME)의 2006~2016년까지 최근 10년간의 연도별 평균 수질 현황이다. 추동지점의 경우 상류에서 주원천이 문의는 품곡천이 유입된다. 연도별 수질 변화를 살펴보면 생분해성 유기물질의 지표인 BOD는 유지 및 관리 되고 있으나 난분해성 유기물질의 영향을 받는 COD는 전반적으로 농도가 높아지는 것을 확인 할 수 있다. 조사기간 동안 농도는 BOD 1.0~1.8 mg/L, COD 2.8~4.7 mg/L로 나타났다. 이처럼 생분해성 유기물을 대표하는 BOD는 어느 정도 개선된 반면, COD와 같은 난분해성 유기물이 높아지고 있다는 것은 수중에 미생물이 분해하기 어려운 난분해성 유기물이 많이 존재하는 것을 의미하는 것으로 문헌연구에서도 호소 내 COD가 높아지는 이유로 HoA와 HiA를 지목한 바가 있어[27] 난분해성 유기물의 관리가 더 필요할 것으로 판단된다.
3.2. 유기물 농도 분포
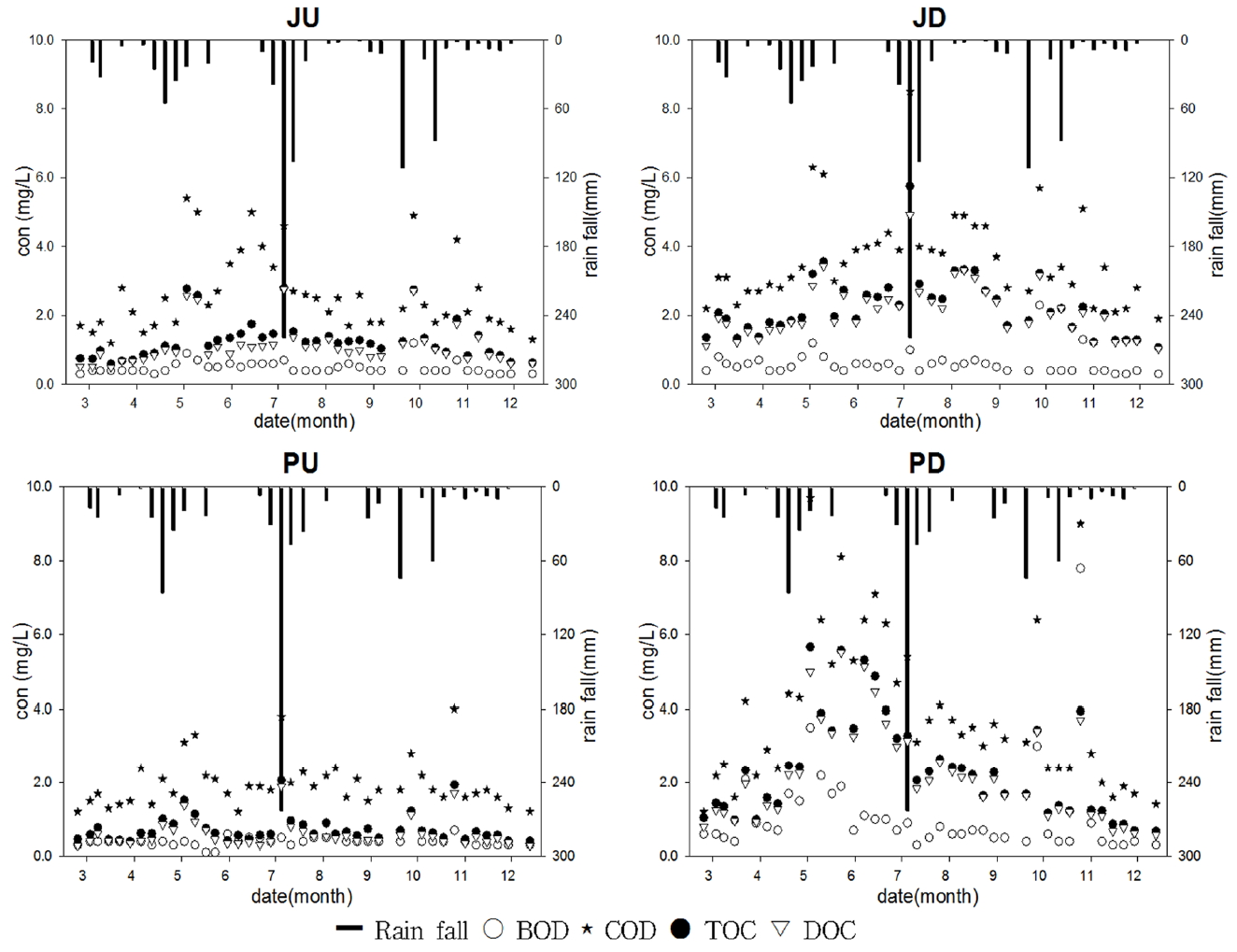
Fig. 3은 주원천과 품곡천 상·하류 지점에 대한 BOD, CODMn, TOC, DOC 및 강우량에 대한 분석 결과이다. 주원천 상류(JU)의 경우 순수 산림 유역으로 변동 되는 것을 확인할 수 있으며, BOD는 평균 0.5 ± 0.2 mg/L, COD는 평균 2.6 ± 1.1 mg/L로 조사되었다. 또한 일일누적 강우량이 23.0 mm이 있었던 시기에 COD가 최대 농도를 보였다. 하류(JD)의 경우 상류에 소규모 저수지(세천지)가 있고 마을을 통과하여 흘러 내려오는 복합피복 유역으로써 COD 농도는 평균 3.7 ± 1.3 mg/L로 상류보다 높았다. 또한 7월 5일에는 강우의 영향으로 최대 측정값을 보였으며 일 강우량은 259.5mm이었다. 주원천의 DOC/TOC 비율은 상.하류 지점에서 상류지점이 87%, 하류지점이 94%로 하류지점이 상류지점에 비해 약 7% 높게 나타났다. 품곡천의 경우 상류지점(PU)은 주원천 상류와 같은 순수산림 유역으로 COD 농도는 평균 2.1 mg/L로 나타났다. TOC 농도가 2.1 mg/L로 최대관측을 보인 7월 5일 측정에서는 약 260 mm 강우의 영향을 받은 것으로 판단된다. 품곡천 하류(PD) 지점 역시 복합 피복 유역으로써 COD 농도는 5월 3일 측정에서 강우의 영향을 받아 최대 측정값(9.7 mg/L)을 보였으며 평균 4.0 mg/L으로 상류보다 약 2배 정도 높았다. TOC는 같은 측정일 최대 5.7 mg/L, 평균 2.4 mg/L로써 상류와 비슷한 수준을 보였다. 품곡천의 DOC/TOC 비율은 상류지점이 80%, 하류지점이 93%로써 상류지점 보다 하류 지점이 약 13% 높았으며, 주원천과 유사한 경향으로 나타났다. 각 하천에서 유기물의 시간적 경향은 생분해성 물질과 난분해성 물질 간 약간 다르게 나타나는 패턴을 보였다. 먼저 생분해성인 BOD의 경우 유량이 다소 적은 갈수기에 높게 나타나는 경향을 보였는데, 특히 2~4월에 대체적으로 높게 나타났으며, 이는 선행연구[28]와도 비슷한 결과로 갈수기 동안 하천의 유량은 줄고, 배출되는 양은 일정하기 때문이다. 또한, 장마가 시작되는 6월부터는 BOD농도가 감소하는데 이는 우리나라의 전형적인 몬순기후의 영향으로 하천에 수량이 풍부해지면서 수체의 안정화로 인해 농도가 감소하는 것이다. 이와는 반대로 COD, TOC는 장마가 시작되는 6월에 높게 나타나는데 이는 장마 기간 발생한 강우 유출로 인해 유기물 증가와 더불어 기저유량도 증가하는데 이중 난분해성 유기물질이 많은 비중을 차지했을 것으로 판단된다.
3.3. 난분해성 물질 특성
친수성(Hi) 물질에 비해 소수성(Ho) 물질이 물과의 친화도가 낮으며 미생물에 의한 분해가 어렵다는 것은 이미 알려져 있는 사실이다. 이는 즉 미생물 섭취가 용이한 친수성을 띠어야 하는데 분해되기 어려운 소수성 물질이 높다는 것을 의미한다. 특히, 대표적인 난분해성 NOM 물질은 리그닌 계열의 방향족 탄소에 –COOH, –OH등의 작용기를 포함하는 지방족 탄화수소 종류로 소수성산(HoA) 성분에 해당하는 Humic 물질이다[29]. 한편, 소수성중성(HoN) 성분은 카르보닐계열 및 지방족 탄화수소의 화합물로서 긴 탄소사슬(>C9)과 여러 개의 방향족 성분을 포함하는 것으로 이러한 사실은 HoA와 HoN 역시 미생물에 의한 분해가 어려운 구조로 되어 있음을 의미한다. 이러한 이유로 국제 휴믹학회(IHSS) 에서는 HoN과 HoA 성분을 포함하는 Ho 성분 전체를 휴믹물질(HS)로 분류하고 있다[30].
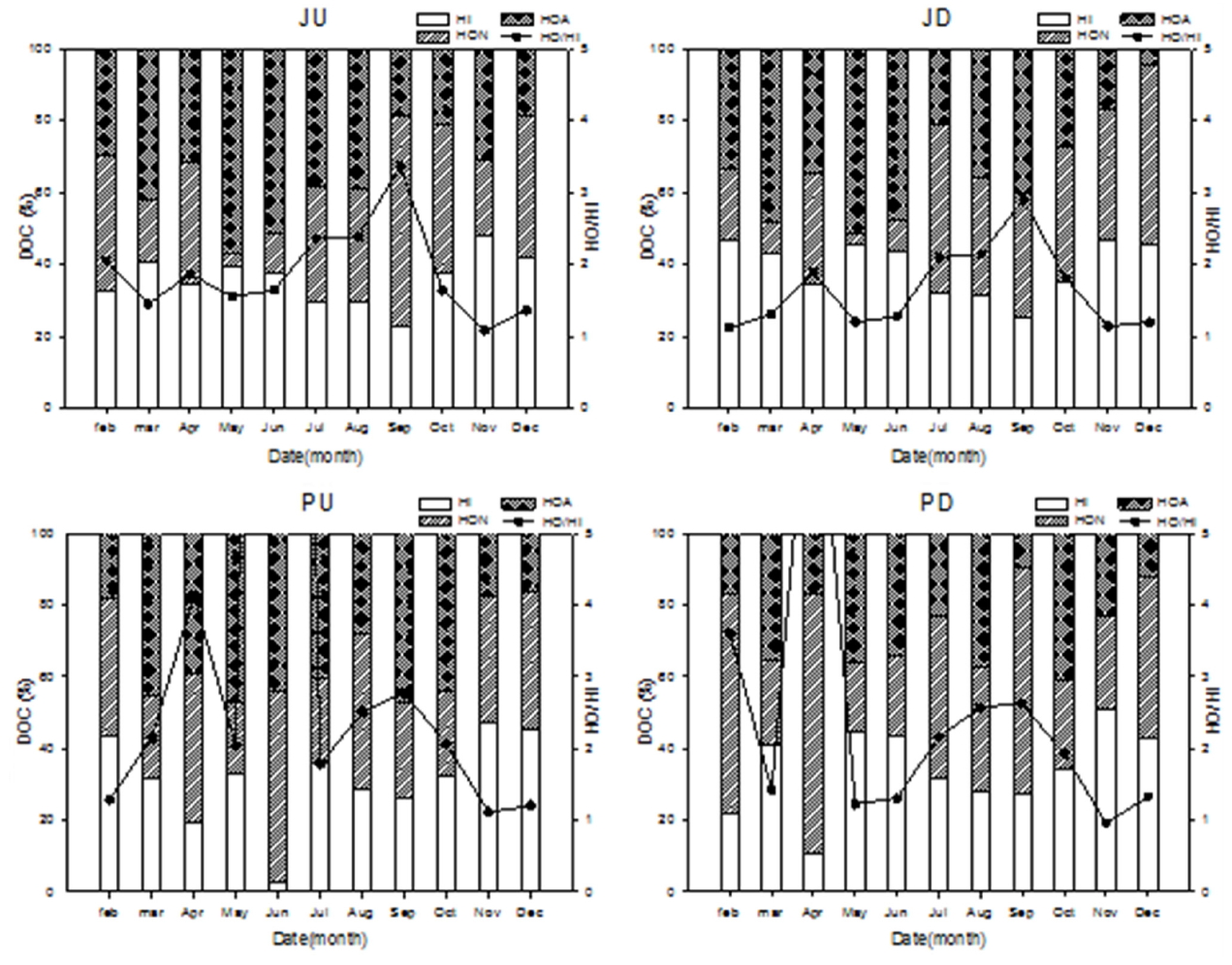
Table 3, Fig. 4는 주원천과 품곡천의 상·하류에 대해 월 1회 resin을 이용하여 분리한 결과를 나타내었다. 전체 DOC(mg/L)중 유기물 성분에 따른 분포 확인을 위해 친수성(Hi) 및 소수성 산(HoA), 소수성 중성(HoN)으로 농도를 나누어 확인 하였다. 주원천 상류(JU)에서는 Hi 0.2~0.7 mg/L, HoN 0~1.6 mg/L, HoA 0.1~0.6 mg/L, 하류(JD)는 Hi 0.5~1.0mg/L, HoN 0.1~1.1mg/L, HoA 0~1.3 mg/L로 분석 되었다. 품곡천 상류(PU)의 경우 Hi 0~0.6mg/L, HoN 0.1~0.4mg/L, HoA 0~0.8mg/L, 하류(PD)는 Hi 0.2~1.5 mg/L, HoN 0.2~2.1 mg/L, HoA 0.1~1.5 mg/L로 분석 되었다. 그 결과 소수성 성분이 전체 DOC에서 주원천의 경우 52.1~77.1% / 품곡천은 52.7~97.1%를 차지하여 소수성이 주요 성분임을 알 수 있었다. 품곡천의 경우 4월에 상. 하류에서 높게 나타난 것은 주원천과 달리 복합유역으로 갈수기 이후 강우(86 mm)로 인한 유기물 증가로 보여지며, 주원천 상류의 경우 집중 강우 시기(7월~9월)에 평균 72.8%가 소수성 성분이고 갈수기 시기에는 평균 60.9%로 강우기에 11% 이상 높게 나타나 강우기 유량 증가로 인해 난분해성 유기물 또한 함께 증가함을 알 수 있으며 모든 조사지점에서 역시 비슷한 경향이 보임을 확인 할 수 있다.
3.4. 형광 EEM 분석결과
형광 EEM 분석은 전체 파장에 대한 형광스펙트럼을 포함하고 있어 전체적인 형광특징을 파악하는데 효율적이다. Fig. 5의 EEM 형광특성 영역을 파악하기 위해 Synchronous 스펙트럼과 같이 4가지로 Table 4에 정리하였다. Fig. 5는 강우기전(3월), 강우기(7월), 강우기후(11월)의 주원천, 품곡천의 상 하류, 추동, 문의 지점에 대한 형광 EEM을 보여주고 있다. 주원천과 품곡천의 형광분석 결과, 주로 휴믹산계 물질의 유입이 관찰되었고 그 외에도 프로테인계 및 펄빅산계 등 다양한 유기물이 유입되는 것을 알 수 있었고, 이는 모든 지점에서 220 nm 여기파장, 440 nm 방출파장에서 비슷한 피크를 보여주고 있으며 형광 세기가 공통된 구조적 특징과 관련이 있음을 의미한다. 조사 기간 중 하천의 경우 강우기인 7월에 형광 세기가 증가하는 것을 확인 할 수 있는데 앞서 resin분석 결과에서도 비슷한 시기에 Ho가 증가하는 것을 알 수 있다. 이후 11월에는 형광세기가 다소 감소하는 것으로 나타났다. 또한, 주원천은 하류보다 상류에서 휴믹산계 형광세기가 관찰되었지만 품곡천은 하류에서 휴믹산계 형광세기가 관찰되는 것으로 보아 하류로 유입되는 유기물이 난분해성일 가능성이 있음을 의미한다. 대청호 내 추동과 문의의 형광분석 결과에서도 휴믹산계 형광특성이 관찰되었으며 지점별 차이는 그리 크지 않은 것으로 나타났으나, 하천과는 상이한 결과로 7월에 형광세기가 감소하는 특성을 보이는데 이는 호소의 특성상 강우기에 유량증가가 비점 유입에 따른 영향일 것으로 판단된다. 또한, 단백질계(220 nm/300~380 nm) 및 미생물 생성(275 nm/325 nm)에서 형광 세기가 관찰되었는데 많은 선행연구 결과에서도 단백질계 형광세기 영역이 뚜렷한 것은 미생물에 의한 분해가 활발할 때 관련이 있는 것으로 보고되었다. 본 조사지점 역시 호소의 특성상 하천에 비해 유기물 성상의 계절적 변화는 적고 조류증식 혹은 미생물에 의한 것으로 판단되며, 유입하천의 하류에 비해 형광세기의 변동 폭은 작으나 강우기인 7월 이후부터 지속적으로 휴믹산계 형광세기가 증가하는 것으로 관찰되었다. 이는 호소 내 미생물의 영향을 많이 받아 결과적으로 유입 하천과는 다른 성상을 나타내는 것으로 생각된다.
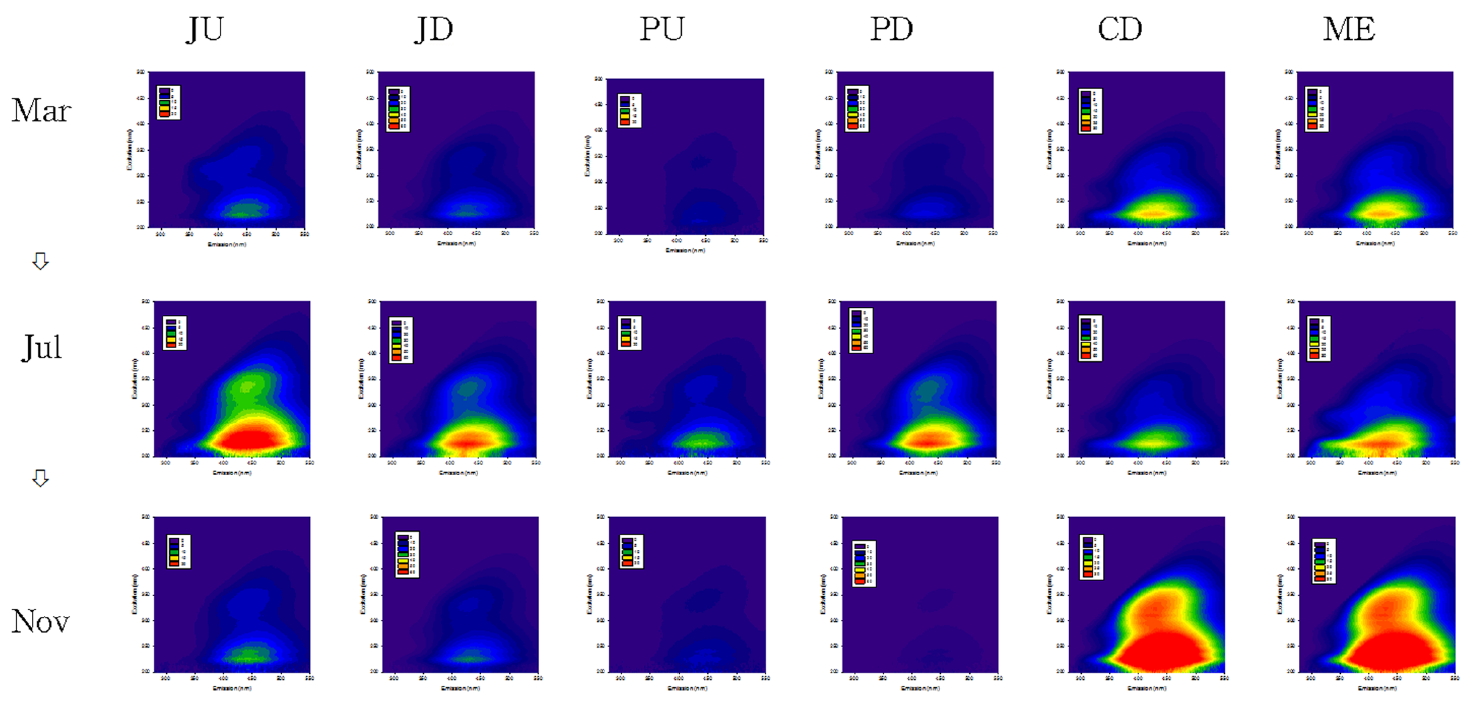
Fluorescence excitation-emission matrix (EEM) of streams and lake DOM. (JU: Juwon upstream, JD: Juwon downstream, PU: Pumgok upstream, PD: Pumgok downstream, CD: Chudong, ME: Munui)
3.5. 상관분석결과
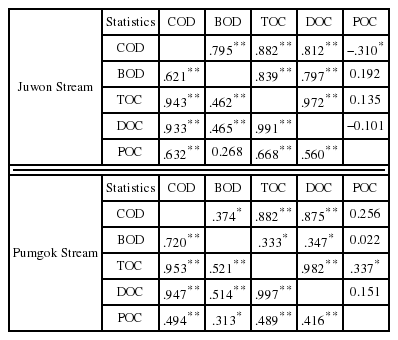
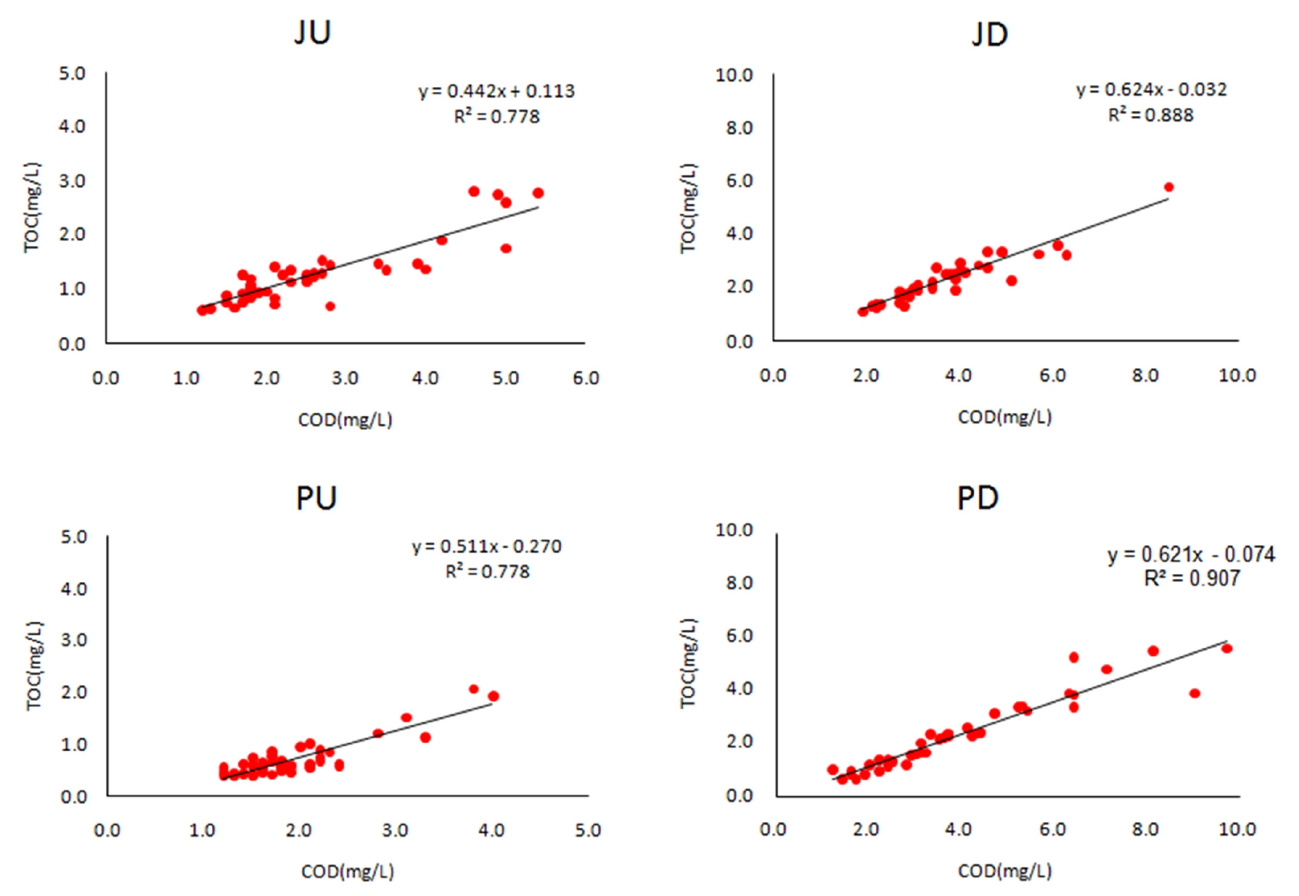
주원천과 품곡천의 상·하류간 유기물 관측자료를 SPSS(ver.18) 통계프로그램을 이용하여 상관관계를 분석하였다(Table 5 및 Fig 6). 주원천의 TOC와 COD의 상관계수는 0.882~0.943(p < 0.01)로 나타나고 품곡천은 TOC와 COD에서 0.882~0.953(p < 0.01)으로 나타나 COD가 BOD보다 TOC와 상관성이 높다는 것을 알 수 있었다. 이처럼 COD보다 BOD가 TOC와 상관성이 낮은 이유는 분해율이 낮으며, 실제로 수중에 난분해성 유기물이 존재하기 때문으로 사료되며, 이는 기존 연구에서 TOC가 BOD보다는 COD와 상관성이 더 높다고 보고한 것과 유사한 결과[31,32]로 Kim et al [28] 연구에서도 본 연구와 유사한 TOC와 COD에서 상관계수는 0.796으로 조사되었다. 특히 모든 지점에서 DOC와 TOC와의 상관계수는 0.972~0.997(p<0.01)로 높게 나타나 산소소모량 기준인 COD 농도에 비해 유기탄소 기반의 유기물 지표가 난분해성물질 농도를 더 잘 반영함을 알 수 있었다. 또한, Fig 6과 같이 산포도상에서의 회귀선은 회귀식으로 나타낼 수가 있으며 기울기는 각각 0.4428, 0.6242, 0.5112, 0.6214로 이는 COD의 단위변화량에 대한 TOC의 변화량으로, 이는 COD가 1 mg/L 증가할 때 평균적으로 TOC가 기울기만큼 증가함을 의미하기도 한다. 또한, CODMn 자료를 이용하여 하천의 난분해성 물질농도 추정이 가능할 것으로 판단된다.
이와 같이 변수간의 상관관계 파악으로 유기물간의 추정이 가능하며 보다 낮은 산화율로 인한 분석 오차를 극복하는 대안으로써 TOC가 유기물 관리 대상 물질로 선정되면 COD와 BOD도 함께 관리 될 수 있을 것으로 사료된다[33].
4. 결 론
본 연구에서는 대청호로 유입되는 지천 중 주원천과 품곡천을 대상으로 XAD 수지분획을 통해 난분해성 유기물의 유입특성을 조사하고, 비교 분석하였다.
일반항목 조사결과, 주원천의 COD는 2.7~3.7 mg/L, TOC는 1.3~2.3 mg/L으로 분석 되었으며, 품곡천에서는 COD 2.1~3.9 mg/L, TOC 0.7~2.4 mg/L으로 상류에서 보다 하류가 높은 결과를 보였다. 또한 DOC/TOC비도 상류지점 보다 하류 지점에서 (주원천 상류 87% < 하류 94%, 품곡천 상류 80% < 하류 93%) 높게 나타나, 이러한 결과는 두 지류 하천에서 유기물 농도가 농업용 저수지를 통과하면서 1차 생산에 따른 내부 난분해성 유기물 유입 영향으로 증가한 것으로 보인다. 반면, POC는 주원천과 품곡천 모두 하류보다 상류에서 높은 농도를 보였는데 이는 산림유역에서 기원한 외부 자연 유기물의 영향으로 판단된다. XAD resin 분석 결과, Ho의 비율이 주원천에서는 전체 DOC의 52.1~77.1%, 품곡천은 52.7~97.1%로 Hi보다 높았다. Ho성분의 유기물은 대부분 유역의 상류 산림지역으로부터 유입하는 Humic acid으로 구분되었으며, 시료에서의 Ho/Hi 비율이 강우기(7월~9월)에 서서히 증가하다가 갈수기 때 감소하는 것으로 보아 Ho성분이 강우-유출을 통해 하천에 유입되는 특성을 확인 할 수 있었다. EEM 형광 분석 결과 하천의 경우 전지점에서 Humic-like 물질이 관찰되었고 특히 강우기에는 유기물질의 유입으로 형광세기 역시 증가하는 특성을 보였으며, 호소의 경우에는 강우기에 유량의 증가와 댐 내부의 미생물의 영향으로 하천과 상반되는 특성을 보이다 갈수기에는 다시 증가하는 특성을 보였다. 난분해성 물질 간 연관성을 확인하기 위한 상관분석 결과 난분해성 유기물 간접지표인 TOC와 COD는 강한 양의 상관성(p < 0.01)을 보였다.
본 연구를 통하여 대청호로 유입되는 지류 하천에 존재하는 난분해성 물질의 성분과 배경 농도 자료를 확보하였지만 향후 대청호를 비롯한 금강 본류의 자연 유기물 관리를 위해 지속적인 조사 연구가 필요할 것으로 판단된다.
Acknowledgements
본 논문은 환경부의 재원으로 2016년 금강물환경연구소의『상수원 이용호소의 산림유래 난분해성물질 거동평가 및 관리 연구』의 일부로 수행하였습니다.(NIER-RP2016-371)