1. 서 론
전세계적으로 수질 중 질산성질소의 오염은 환경문제로 우려가 되고 있는 물질 중의 하나이며 자연적인 질소 순환, 축산폐수, 그리고 화학 비료 등에 의해 생성되며 잠재적으로 지표수와 지하수 중에 높은 농도의 위험한 수준으로 나타나기도 한다[1,2]. 질산성질소로 인한 피해를 막기 위해 미국 환경보호청(Environmental Protection Agency, EPA), 세계보건기구(World Health Organization, WHO), 유럽공동체(European Union, EU) 에서 먹는 물에 대한 질산성질소의 농도를 각각 10 mg L-1, 10 mg L-1 그리고 50 mg L-1 이하로 규제하고 있다[3]. 우리나라의 경우 먹는물 수질기준 및 검사 등에 관한 규칙으로 먹는물에 대하여 질산성질소의 농도가 10 mg L-1를 넘지 않아야 한다고 규정하고 있다[4]. 질산성질소에 의한 오염 예방 및 오염원 유입 경로 파악을 위해 질산염의 질소 동위원소 값이 연구 분야에 활용되고 있다[1,5-8].
질산염의 질소 안정동위원소비(δ15N)는 일반적으로 화학비료(−3.9‰ ~ 0.5‰), 토양 유기물(2‰ ~ 9‰) 그리고 가축분뇨(6.8‰ ~ 20.9‰)의 영향에 따라 상이한 값을 나타내므로 수질 시료의 질소 안정동위원소비는 오염원을 추적할 수 있고 또한 오염원의 기여도를 평가하는 도구로도 활용되고 있다[5,6,9-11]. 그러나 오염원별 질소 안정동위원소 값이 서로 중첩되는 범위가 존재하고 있어 질소 안정동위원소비만을 이용하여 오염원을 추적하는 것은 어려움이 있다[11]. Curt et al. (2004)은 5.9‰~ 36.7‰의 범위로 나타나는 가축분뇨의 질소 안정동위원소비가 4.6‰ ~ 20.2‰의 범위로 나타나는 생활하수의 질소 안정동위원소비를 이용한 질산성질소 오염원 인자 판별의 한계를 보고하였다[1]. 이러한 한계를 극복하기 위해 탄소, 질소, 수소 그리고 산소와 같은 다중원소들의 안정동위원소비 분석을 통하여 원산지 판별[12]과 질산염의 δ15N와 δ18O를 함께 활용한 오염원 추적 연구가 진행 되고 있다[10,12-14].
한편, 1980년대 이후로 질산염의 δ15N와 δ18O를 동시에 분석하는 방법에 대한 연구가 보고되었다[15-18]. 특히, 아산화질소 환원 효소가 부족한 탈질 미생물을 이용하여 물속의 질산염(NO3-)을 N2O가스로 환원시키고 이 가스를 이용하여 δ15N와 δ18O를 동시에 분석하는 방법은 Sigman et al. (2001)에 의해 처음 소개되었으며 [19] 현재 질산염의 δ15N와 δ18O분석에 많이 이용되고 있 다[20,21].
본 연구에서는 조사지점의 상수유역 오염원의 δ15N와 δ18O에 대한 시공간별 변화양상에 대해 파악하고자 축산폐수, 화학비료 등 오염원 구분이 비교적 뚜렷한 6개의 지점에서 2년간 수질 중 질산염의 δ15N와 δ18O를 측정하여 상수원수 오염원을 조사하였고 상수원수에 미치는 오염원의 기여율도 초보적으로 산출하였다. 본 연구에 의해서 상수원수 수질관리에 도움이 될 것으로 판단한다.
2. 재료 및 방법
2.1. 조사지역
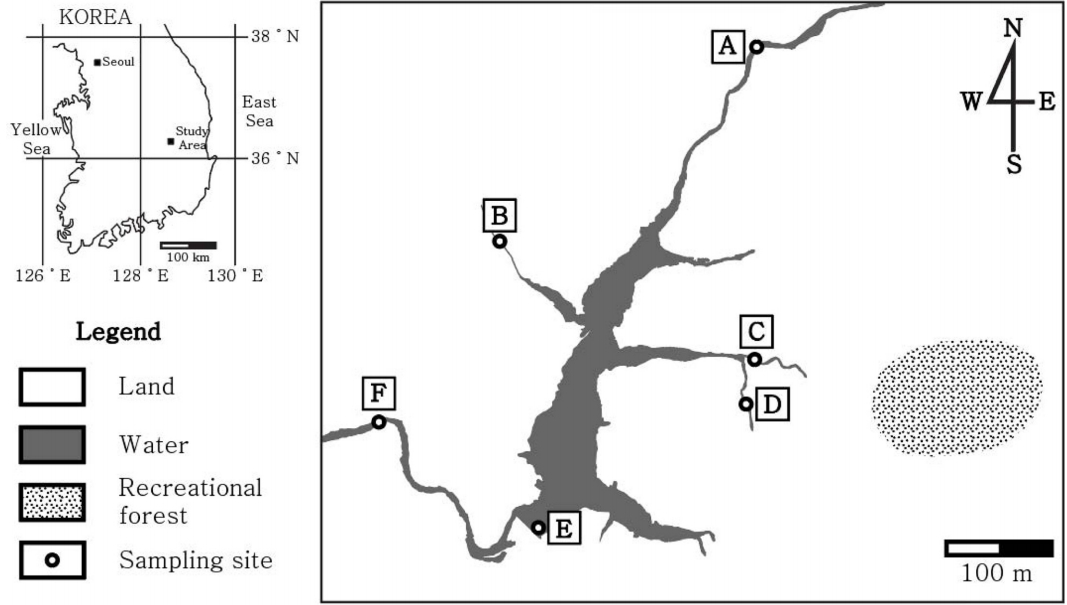
상수원은 깨끗한 물을 필요한 수량만큼 취수 하려는 상수도 계획에서 수원 선정 시 수질, 수량, 급수지역과의 거리, 공사 난이도, 시설비와 유지관리, 장래 확장 가능성을 고려하여야 하는데 수원의 조건으로는 가능한 주위에 오염원이 없어야 하며, 수질이 양호하고 수량이 풍부하여야 하며 계절적으로 수량 및 수질의 변동이 적어야 한다. 본 연구에서의 조사 지역인 군위댐은 상수원으로 상시 수질 및 수량 모니터링, 오염원 유입 차단, 상수원 주변 환경관리 등 엄격한 수질관리가 이루어지는 지역이다. 군위댐 주변의 인가, 경작지, 그리고 축사 등 상대적으로 오염원의 특성이 뚜렷한 4곳 (유입천 A, B, C, D), 상수원 저수지 (E), 상수원 하류 (F) 총 6지점을 선정하였으며, 2년간 총 8회의 샘플을 채취하여 질소와 산소 안정동위원소비 분석을 수행하였다 (Fig. 1).
샘플 채수 지점 6곳의 특성은 A지점 (DG)의 경우, 상수원 저수지로 군위댐에 가장 많은 수량이 유입되는 하천이며 본 조사 지역에서 가장 많은 인가와 경작지 (과수원, 밭 등)가 형성되어 있다. 유입천 상류 지역에 오래 전 가행 되었던 광산이 존재하나 지금은 폐광한 후 오염원 유출이 차단된 것으로 판단되었다. B지점 (YA)은 상류에 과수원이 형성되어 있으며, 가축 축사가 설치되어 있다. 현재 가축은 사육되고 있지 않으나 과거 가축 사육 시 누적되었던 가축 분뇨 오염물이 존재하며 가축 분뇨의 누출로 인한 오염 가능성이 예상되는 지점이다. C지점 (JG1)과 D지점 (JG2)은 상류에 몇몇의 인가와 과수원 그리고 자연휴양림이 위치한다. 자연휴양림의 경우 상하수도 배관이 잘 설비되어 있어 오염물질이 직접적으로 상수원에 유입될 가능성은 적어 보인다. 그러나 과수원에서 화학 비료 등 오염물질에 노출이 용이하며 인가에서 나오는 오수가 하천으로 유입되어 이로 인한 오염 가능성을 고려할 수 있다. E지점 (KWD)은 상수원 저수지이며 상류의 여러 유입천에서 오염물질이 유입되기 때문에 각 지점별 오염원 특성과 시기별 특성을 종합적으로 고려하여야 한다. F지점 (IGS)의 경우 상수원 저수지의 하류에 위치하고 있으며 저수지에서 본 지점 사이에 휴양시설이 있으나 이로 인한 영향은 미미할 것으로 예상된다.
2.2. 안정동위원소비 분석방법
질소와 산소의 안정동위원소비는 탈질법을 이용한 질산염의 δ15N와 δ18O 분석법을 적용하였다[20]. 시료 분석은 안정동위원소 질량분석기 (IR-MS; stable isotope ratio mass spectrometer, 한국기초과학지원연구원(KBSI) 소재)로 분석하였다.
탈질 미생물에 의해 생성된 아산화질소를 분리 정제하기 위하여 미량가스 농축기인 Trace Gas System (Isoprime, UK)을 사용하였다. 분석된 원소들의 안정동위원소비는 천분율(‰)로 나타내고 델타표시법(δ)을 적용하였다.
여기서 15N/14N는 대기 중 질소, 18O/16O는 Vienna Standard Mean Ocean Water (VSMOW)에 의해 보정된 값을 사용하였으며 correction factor법을 사용하여 보정하였다. 안정동위원소 분석의 신뢰도를 높이기 위하여 세계적으로 널리 이용되는 표준물질인 IAEA-NO3 (Potassium Nitrate, International Atomic Energy Agency), USGS-34 그리고 USGS-35(Potassium Nitrate, U.S. Geological Survey)를 사용하여 측정값을 보정하였다.
표준물질 IAEA-NO3의 권고 값은 δ15NAIR = 4.7 ± 0.3‰, δ18OVSMOW = 25.6 ± 0.4‰이고 표준물질 USGS-34와 USGS-35의 권고 값은 각각 δ15NAIR = −1.8 ± 0.1‰, δ18OVSMOW = −27.9 ± 0.3‰와 δ15NAIR = 2.7 ± 0.1‰, δ18OVSMOW = 57.5 ± 0.3‰이며 본 실험에서 측정된 표준물질의 평균값은 권고 값 범위 내로 측정되었다.
2.3. 오염원별 기여도 평가
동위원소 혼합 모델(two-sources isotope mixing model)을 이용하여 각 오염원의 상대적 기여도를 계산하였다[22].
여기서 % NDFF는 수질 시료 전체 NO3− 중 화학비료에서 유래된 양의 백분율, δ15NO는 가축분뇨 기원 질소의 δ15N, δ15NF는 화학비료의 δ15N, δ15Nw는 수질 시료 중 NO3−의 δ15N값이다. % NDFF는 (유기성 오염물질 기원 질소)의 비율은 100% NDFF로 계산하였다. 위 식은 동일 지점에서 시간에 따른 오염원 기여도의 상대적 변화 또는 동일 시점에서 지역 간 오염원 기여도의 상대적 차이를 추정하기 위한 것으로 δ15NF와 δ15NO는 연구 지역의 오염원 특성에 따라 다양한 값을 적용시킬 수 있다. 본 연구는 Choi et al.(2007)에 의해 제시된 화학비료의 동위원소 값 범위 중 가장 높은 값인 0.5‰과 가축분뇨의 동위원소 값 범위 중 가장 낮은 값인 6.8‰을 각각 δ15NF와 δ15NO으로 사용하였다[5].
3. 결과 및 고찰
3.1. 수질 중 질소(δ15N)와 산소(δ18O) 안정동위원소비 변화
본 연구에서 조사한 6지점의 수질시료를 2년간 총 10회 측정한 질소(δ15N)와 산소(δ18O) 안정동위원소 값을 Table 1에 나타내었다. 2016년부터 2017년까지 샘플 채취 지점 6 곳의 질소(δ15N) 안정동위원소 값의 평균은 5.7‰로 나타났다. 본류인 A지점은 저수지인 E지점으로 유입되는 유량이 가장 많고 E지점의 δ15N 변화와 비슷한 양상을 보여 E지점에 가장 많은 영향을 주는 지점으로 보인다. B지점은 2016년 6월과 2017년 6월에 δ15N이 B지점의 평균보다 7.9‰ ~ 10.0‰ 높게 나타났고, C지점은 2016년 6월에는 δ15N이 평균보다 높은 14.2‰로 나타났지만 2017년 6월에는 평균보다 낮은 -7.0‰로 나타났다. B지점과 C지점의 극단적인 동위원소 비의 차이가 저수지인 E지점의 δ15N에 영향을 거의 주지 않는 것으로 보인다. D지점 δ15N 값의 평균은 2.4‰로 다른 지점의 δ15N 값과 비교해 1.4‰ ~ 5.6‰ 낮은 값을 나타내지만 E지점으로 흘러 들어가는 유량이 적어 E지점의 δ15N에 크게 영향을 주지 않는 것으로 사료된다. F지점은 E지점의 직하류로 E지점 δ15N 값의 변화양상과 비슷하게 나타난다.
2016년부터 2017년까지 샘플 채취 지점 6 곳의 산소(δ18O) 동위원소 값의 평균은 3.4‰으로 나타났다 (Table 1). 전반적으로 6개 지점의 비슷한 변화양상이 관찰되나 2016년 6월에는 B지점(22.7‰), C지점(21.1‰), D지점(13.7‰) 모두 높은 δ18O이 나타났으며 2017년 6월에는 D지점(−2.7‰)만 낮은 δ18O이 나타났다. δ18O 값의 변화를 통해 E지점의 산소 안정동위원소 값은 A지점과 B지점의 영향을 받는 것으로 유추하였다. A지점의 경우 E지점으로 유입되는 유량이 많아 δ18O 값의 변화가 가장 유사하게 나타났다. 반면 A지점보다 E지점으로 유입되는 유량이 작은 B지점의 경우도 E지점의 δ18O값의 변화와 유사하게 나타났다.
군위댐 유역 6개 지점의 δ15N와 δ18O는 대부분 토양 기원의 범위 내에 도시되어 토양 유기물에서 유래된 질산염의 영향을 받는 것으로 나타났다 (Fig. 2). 하지만 군위댐 주변의 end-member를 확보하여 비교하지 않았기 때문에 더욱 정확한 정보를 얻기 위해서는 환경다매체 분석도 필요할 것으로 판단되었다. B지점과 C지점에서 화학비료의 범위와 축산폐수에 의한 범위로 나타나는 극단 값으로 특정 오염원의 영향을 받고 있음을 유추하였다. B지점의 경우 2016년 6월 δ15N(15.1‰)과 2017년 6월의 δ15N(17.2‰)은 뚜렷하게 높은 값을 나 타내어 B지점은 축산폐수에서 유래된 오염물질의 영향을 받고 있는 것으로 사료된다. 반면 C지점은 2016년 6월에는 δ15N(14.2‰)이 높은 값을 나타내지만 2017년 6월에는 δ15N(-7.0‰)이 낮은 값을 나타내는 것으로 유추해 볼 때, C지점은 축산폐수의 영향과 화학비료의 영향을 동시에 받고 있는 것으로 판단된다. 그러나 C지점은 인가나 축사가 위치하지 않고 자연휴양림이 위치하나 상하수도 시설 잘 갖추고 있기 때문에 오염원 유입에 대한 우려가 적으므로 인접한 D지점의 인가와 과수원에서 유입된 오염원의 영향을 받았을 가능성도 배제 할 수 없다. 따라서 2017년 6월 C지점의 δ15N값이 과수원이 밀집한 D지점의 δ15N값보다 낮은 것은 C지점과 D지점이 서로 인접하고, 상대적으로 지대가 낮은 C지점에 화학비료 기원 오염원이 유입되었을 것이라고 추측되었다.
Broadbent et al.(1980)은 경작지 토양의 δ15N값(0.65 ± 2.6‰)과 비경작지 토양의 δ15N값(2.73 ± 3.4‰)을 보고[23] 하였으며 이와 비교하여 분석해 볼 때 본 연구지역의 δ15N값(mode: 3.5 ~ 7.3‰; mean: 5.7‰)은 비경작지 토양 유기물에서 유래된 질소 값의 범위 내로 나타나므로 자연발생적인 토양 유기물의 영향이 지배적인 것으로 사료된다 (Fig. 3). D지점은 비경작지 토양 범위와 경작지 토양의 범위에 중첩되어 도시되나 과수원이 밀집되어 있는 점을 고려할 때 경작지 토양의 범위에 더 가까울 것으로 판단된다.
암모늄이온(NH4+)에서 질산이온(NO3−)으로 산화될 때, 질소원자는 물(H2O)에서 유래된 산소 원자 2개와 물속에 녹아 있는 대기 중 산소(O2)에서 유래된 산소 원자 1개와 결합하여 질산이온으로 산화되며 질산염의 δ18O 값은 질산이온이 생성될 때의 물과 대기의 환경을 반영한다[11,24]. Wassenaar(1995)는 δ18O값이 다른 질산염 기원 물질로부터 합성 질산염 비료의 영향을 구별할 수 있어 질산염의 기원을 규명하는 좋은 추적자임을 제안하였다[25]. 본 연구지역인 6개 지점의 δ18O값은 B지점과 C지점의 극단 값을 제외하고 대부분 질산화 과정의 범위로 나타났다 (Fig. 3). B와 C지점의 극단 값이 질산염 비료의 범위에 나타나더라도 각각 15.1‰과 14.2‰로 나타나는 δ15N값을 고려할 때 6개 지점의 δ18O는 화학비료, 토양 유기물과 가축분뇨의 영향을 포함하는 질산화 과정의 영향으로 판단된다. E지점에서 다른 지점보다 전반적으로 높은 δ18O값이 나타나는 것은 저수지에서 나타나는 증발효과(evaporation) 또는 호흡 분별작용(respiratory fractionation)에 의한 결과로 추측된다[24].
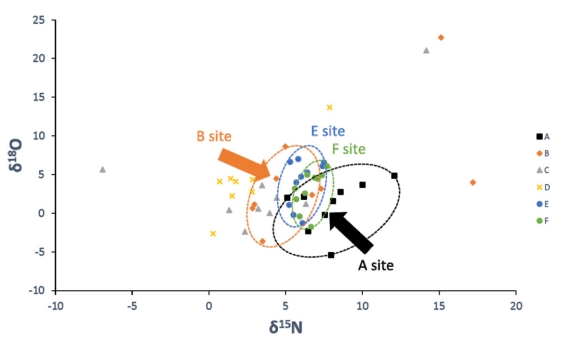
δ15N와 δ18O의 상관관계로부터 E지점과 F지점은 A지점과 B지점의 영향을 혼합하여 받는 것으로 나타났다 (Fig. 4). E와 F지점의 δ15N와 δ18O값의 영역은 A와 B지점의 영역과 가장 유사하고 A와 B지점의 영역 사이에 E와 F지점의 영역이 위치하여 A지점의 영향과 B지점의 영향이 혼합하여 나타난 양상을 보인다. A지점은 E지점으로 유입되는 유량이 많고 δ15N와 δ18O값의 변화가 E지점과 F지점과 유사하게 나타나므로 A지점의 영향이 크게 작용한다고 판단할 수 있고, B지점의 경우 2016년과 2017년 6월에 나타나는 극단 값을 제외하고는 E와 F지점의 변화와 유사하게 나타나는 것으로 B지점의 영향 또한 A지점과 함께 작용하는 것으로 판단된다.
3.2. 강우량과 질소(δ15N)와 산소(δ18O) 안정동위원소 비의 상관관계
우리나라는 장마기간 동안 집중되는 강우로 인하여 많은 오염물질의 유입이 예상되어 강우량과 δ15N와 δ18O의 상관관계를 통해 오염물질 유입의 영향을 알아보았다 (Fig. 5). 토양 표면까지 이르는 대기의 질소는 대부분 질산염의 형태로 존재하며[24], 질산염의 경우 강우에 의해 유입 될 수 있기 때문에 비록 채수한 기간에 강우량이 적더라도 취수일정 전 강우가 있었을 경우 강우에 의한 영향이 결과 값에 나타날 수 있을 것으로 판단된다. 2년 동안 군위댐 유역의 강우량 변화는 2016년과 2017년 6월에 특징적인 가뭄이 나타났고 7월에는 많은 양의 강우가 나타났으며 6월과 7월의 강우량의 변화에 따라 δ15N와 δ18O값도 변화하는 양상이 확인되었다. 2016년 6월과 2017년 6월 B지점에서 나타나는 높은 질소 안정동위원소 값, 2016년 6월 C지점에서 나타나는 높은 δ15N값 그리고 2017년 6월 C와 D지점에서 나타나는 낮은 δ15N값을 통해 축산폐수기원 오염원과 화학비료기원 오염원의 영향이 크게 나타난 것으로 판단되지만 2016년과 2017년 7월 많은 강우와 함께 각 오염원의 영향이 거의 나타나지 않고 6개 지점의 δ15N와 δ18O값은 어떤 특정한 값으로 수렴하는 경향을 보여주었다. 이는 강우에 의해 특정 물질의 질산염이 대량으로 유입되는 것으로 보이며 강우량이 많은 시기의 6개 지점의 δ15N와 δ18O값의 범위는 토양 유기물의 δ15N와 δ18O값의 범위로 나타났다.
한편, 우리나라에서 측정된 강우 질산염의 δ15N와 δ18O값은 각각 -1.5‰ ~ 0.2‰와 49.3‰ ~ 54.8‰로 보고되기 때문에 결과 값의 변화가 강우에서 유래된 질산염에 기인한다고 보기는 어렵다[26]. 그러나 강우로 인해 토양 유기물 및 오염물질의 질산염이 용해되어 각 지점의 하천에 유입될 수 있으며 강우로 인해 용해되어 각 지점으로 유입되는 질산염은 토양 유기물 기원의 질산염으로 판단된다. 2016년과 2017년 6월 B, C 그리고 D지점에서 나타나는 특징적인 안정동위원소 값의 영향이 E지점에서 거의 나타나지 않는 것은 2016년과 2017년 6월 가뭄으로 인하여 E지점으로 유입되는 유량이 매우 적었기 때문에 E지점에서 B, C 그리고 D지점의 영향이 나타나지 않은 것으로 판단되었다. 만약 토양 유기물 이외에도 B지점과 C지점이 강우로 인해 기존에 유입되지 않던 오염물질이 다수 유입되어 안정동위원소 조성에 영향을 받았더라도 저수지인 E지점의 동위원소값과 뚜렷한 상관관계가 발견되지 않는 점과 저수지로 흘러 들어가는 유량이 적은 점을 고려해볼 때 강우로 인해 유입된 B지점과 C지점의 오염물질의 δ15N는 토양 유기물의 지배적인 영향 속에서 E지점의 질소 안정동위원소 비에 큰 영향력을 행사하지 않는 것으로 판단하였다.
3.3. 각 지점별 오염원의 기여도 평가
기여도를 평가하는 지표로 질소 안정동위원소 값 이외에 산소 안정동위원소 값 등 다른 수질데이터를 고려해 볼 수 있으나 δ18O값만으로 가축분뇨와 화학비료의 영향을 구분하기는 어려운 점이 있고[11], 이전의 연구에서 다른 항목의 수질 데이터와 δ15N와 δ18O값의 특별한 상관관계는 관찰되지 않는다고 보고하였다[21]. 따라서 δ15N값 이외에 다른 수질 데이터를 사용하여 세부적인 오염원별 기여도를 평가하는 방법에 대한 연구가 향후 필요할 것으로 보인다.
군위댐 유역의 주 오염원인 가축분뇨와 화학비료의 δ15N값에 대해 동위원소 혼합 모델(two-sources isotope mixing model)을 이용하여 각 오염원의 상대적 기여도를 나타내었다 (Table 2). 기여도 평가에 사용된 δ15NF와 δ15NO값은 각각 화학비료와 가축분뇨의 δ15N를 나타낸 것으로 각각의 값은 기존 연구 등에 의하여 다양하게 나타나고 있으나[1,27,28], 본 연구에서는 Choi et al. (2007)이 제시한 국내 화학비료 및 가축분뇨의 δ15N값인 0.5‰과 6.8‰을 각각 δ15NF와 δ15NO으로 사용하여 기여도를 산정하였다[5]. 화학비료의 기여도는 C, D지점에서 크게 나타나며 특히 D지점에서 화학비료의 영향을 많이 받는 것으로 나타났다. C지점과 D지점은 다른 지점들과는 다르게 각 지점 주변으로 과수원이 위치하며 화학비료의 기여도가 높게 나타나는 것은 과수원에서 사용된 화학비료의 영향으로 보인다. 가축분뇨의 기여도는 A지점과 B지점에서 높게 나타나며 A지점에서 가축분뇨는 계절 및 연도에 상관없이 높은 영향을 끼치는 것으로 나타났다. B지점과 C지점에서 각 오염원에 대한 기여도가 유동적으로 나타나는 것을 통하여 두 지점에서 가축분뇨와 화학비료의 영향을 동시에 받아 동위원소적 혼합(isotopic mixing)이 일어나고 있음을 암시한다. 2년 동안 저수지인 E지점과 직하류인 F지점에 대한 가축분뇨의 기여도가 크게 나타나는 것은 상대적으로 E지점으로 유입량이 많은 A지점의 영향에 따라 가축분뇨의 기여도가 큰 것으로 조사되었다. 군위댐 유역의 주 오염원은 가축분뇨 및 화학비료로 크게 나타나고 있으나 군위댐 저수지와 군위댐 직하류에 직접적으로 영향을 주는 오염원은 가축분뇨로 판단된다.
4. 결 론
국내 상수원 유역의 오염원 추적 및 오염원별 기여도 평가를 위해 군위댐 유역 내 오염원이 비교적 뚜렷한 4개의 유입천(A, B, C, D지점)과 군위댐 저수지(E지점) 그리고 하류(F지점)을 대상으로 수질 시료 중 질산염의 질소(δ15N)와 산소(δ18O) 안정동위원소를 분석하여 다중원소의 상관관계로 해석하였다. 각 지점별 δ15N와 δ18O의 평균값은 각각 A지점이 8.0‰과 1.0‰, B지점이 7.2‰과 4.8‰, C지점이 3.6‰과 3.6‰, D지점이 2.4‰과 4.1‰, E지점이 6.1‰과 4.0‰, 그리고 F지점이 6.6‰과 3.1‰로 나타났으며 대부분 토양 기원의 범위에 도시되었고 경작지 토양에서 유래된 유기물보다 자연발생적인 토양 유기물의 영향이 지배적인 것으로 나타났다. 저수지와 하류인 E, F지점의 δ15N와 δ18O값은 비슷하게 나타났으며 두 지점의 계절별 및 연도별 δ15N와 δ18O의 변화 양상은 A지점과 B지점의 변화양상과 비슷하게 나타났으며 상대적으로 δ15N의 높은 값과 낮은 값이 나타났던 B, C, D지점의 변화에는 크게 영향을 받지 않는 것으로 확인되었다.
주 오염원인 가축분뇨와 화학비료에 대한 기여도를 평가한 결과, A지점, B지점은 가축분뇨에 대한 기여도가 크게 나타났으며 C지점, D지점은 화학비료에 대한 기여도가 크게 나타났다. 하지만 B지점과 C지점은 특정 오염원뿐 만 아니라 각각 오염원별 기여도가 유동적으로 나타나며 이는 가축분뇨와 화학비료의 영향을 동시에 받고 있음을 암시한다. E와 F지점은 A지점과 같이 전체 기간 동안 가축분뇨의 기여도가 높고 화학비료의 기여도가 낮은 양상을 보여 A지점의 영향이 가장 큰 것으로 나타났다. 하지만 δ15N와 δ18O의 상관관계를 통해 군위댐 저수지(E지점)와 직하류(F지점)는 A지점의 영향뿐만 아니라 이와 함께 B지점의 영향을 동시에 받고 있는 것으로 나타났다. B지점은 2016년과 2017년 6월 갈수기에서 나타나는 극단 값을 통해 가축분뇨의 오염을 받고 있음을 나타내지만 2016년과 2017년 7월 장마기간 동안 강우로 인해 가축분뇨보다 토양 유기물 기원의 질산염이 대거 유입되면서 E지점에 영향을 주는 것으로 판단된다. 따라서 군위댐 저수지 E지점으로 유입되는 하천 A, B, C 그리고 D지점 중 A와 B지점의 영향이 가장 크게 나타나며, A와 B지점에 대한 정기적이고 지속적인 모니터링을 통하여 향후 수질 관리에 있어 효율적인 방안을 제시할 수 있을 것으로 보인다.